
ISSN 1666-7948
Revista Electrónica de Ciencia y Educación
Departamento de Química Biológica FCEN-UBA IQUIBICEN

ISSN 1666-7948
Revista Electrónica de Ciencia y Educación
Departamento de Química Biológica FCEN-UBA IQUIBICEN
La viruela del mono
Carlos Alberto Bueno
Laboratorio de Virología: Agentes antivirales y citoprotectores. Departamento de Química Biológica. Facultad de Ciencias Exactas y Naturales. Universidad de Buenos Aires. IQUIBICEN- CONICET
Resumen
La viruela del mono (MPX) es una enfermedad zoonótica y actualmente es la infección por ortopoxvirus más prevalente en humanos después de la erradicación de la viruela y el cese de la vacunación antivariólica universal. MPX probablemente se mantiene en la naturaleza a través de la circulación entre varios mamíferos, con eventos indirectos ocasionales para los humanos. La mayoría de los casos de MPX en humanos experimentan síntomas de leves a moderados. La tasa de letalidad varía de 0% a 11% en brotes en áreas endémicas, afectando principalmente a niños pequeños. El tratamiento es principalmente sintomático y de apoyo. Los antivirales tecovirimat, brincidofovir y cidofovir son opciones potenciales para casos severos. La vacunación previa contra la viruela puede conferir protección cruzada contra MPX. Actualmente no hay ninguna vacuna autorizada contra MPX, pero la vacunación temprana posterior a la exposición (dentro de los cuatro días de la exposición a un caso de MPX) con la vacuna contra la viruela puede prevenir la enfermedad o hacer su curso menos grave. Entre humanos, el virus puede transmitirse por vías respiratorias durante el contacto directo y prolongado cara a cara. Además, el MPX puede ser transmitido por contacto directo con fluidos corporales de una persona infectada, o con objetos contaminados con virus. MPX rara vez se exporta desde el continente africano. Sin embargo, recientemente, el 7 de mayo de 2022, el Reino Unido notificó un caso importado MPX en una persona que viajaba de Nigeria. Hoy, la prevalencia de los casos de MPX continúa aumentando en todo el mundo. En este sentido, la Organización Mundial de la Salud ha declarado la MPX como emergencia sanitaria mundial el 23 de Julio del 2022, instando a los gobiernos a tomar medidas coordinadas para detener la propagación del virus.
Palabras clave: viruela del mono, virus, propagación viral.
Monkeypox
Summary
Monkeypox (MPX) is a zoonotic disease and is currently the most prevalent orthopoxvirus infection in humans after the eradication of smallpox and the cessation of universal smallpox vaccination. MPX is probably maintained in nature through circulation among various mammals, with occasional spillover events to humans. Most human cases of MPX experience mild to moderate symptoms. The case-fatality rate of MPX ranges from 0% to 11% in outbreaks in endemic areas with mortality mostly affecting. young children. Treatment is primarily symptomatic and supportive. The antivirals tecovirimat, brincidofovir, and cidofovir are potential options for severe cases. Previous smallpox vaccination may confer cross-protection against MPX. There is currently no licensed vaccine against MPX, but early post-exposure vaccination (within four days of exposure to an MPX case) with smallpox vaccine may prevent the disease or make its course less severe. Between humans, the virus can be transmitted through the respiratory tract during direct and prolonged face-to-face contact. In addition, MPX can be transmitted by direct contact with fluids of an infected person, contact with mucous membranes or non-intact skin with open skin lesions, or with virus-contaminated objects. MPX is rarely exported from the African continent. However, as recently as May 7, 2022, the UK reported an imported MPX case in a person traveling from Nigeria. Today, the prevalence of MPX cases continues to increase worldwide. In this sense, the World Health Organization has declared MPX a global health emergency on July 23, 2022, urging governments to take coordinated measures to stop the spread of the virus.
Keywords: monkeypox, virus, virus spreading
La viruela del mono (MPX) es una enfermedad zoonótica y actualmente es la infección por ortopoxvirus más prevalente en humanos después de la erradicación de la viruela y el cese de la vacunación antivariólica universal [1-3]. El nombre “viruela del mono” se debe al hecho de que el virus infecta a los primates y se aisló inicialmente de un mono de laboratorio en la República Democrática del Congo en 1970 [4].
MPX probablemente se mantiene en la naturaleza a través de la circulación entre varios mamíferos, incluyendo ardillas, ratas gambianas (Cricetomys gambianus), ratones rayados, lirones y primates [5], con eventos indirectos ocasionales para los humanos [6-9]. En áreas endémicas, el MPX se transmite a los humanos a través de una mordedura o contacto directo con sangre, carne, fluidos corporales o lesiones cutáneas/mucosas de un animal infectado [1]. Los casos humanos de MPX son reportados cada vez más en varios países africanos después de su primera identificación, debido a una combinación de factores que incluyen una mayor exposición (deforestación, conflicto y desplazamiento), así como una mejor vigilancia y capacidad de laboratorio en la región de África [4,5,10].
El período de incubación del virus de MPX puede oscilar entre 5 y 21 días, con un promedio de una semana entre la infección y la aparición de los síntomas [5,11]. Los síntomas iniciales generalmente incluyen fiebre, ganglios linfáticos inflamados, dolor de cabeza y dolores musculares; y estos síntomas son seguidos por una erupción cutánea distintiva que consiste en vesículas claras llenas de líquido. Las vesículas finalmente se llenan de pus y finalmente se forman costras para dar paso a una nueva capa de piel sana. Los primeros síntomas son similares a los de la varicela, que es causada por el virus varicela-zoster (un herpesvirus, no relacionado con los poxvirus). Sin embargo, a diferencia de las lesiones de la varicela, que pueden existir individualmente en diferentes etapas de desarrollo a lo largo del curso de la infección, las lesiones de MPX generalmente aparecen, progresan y desaparecen juntas [5,11].
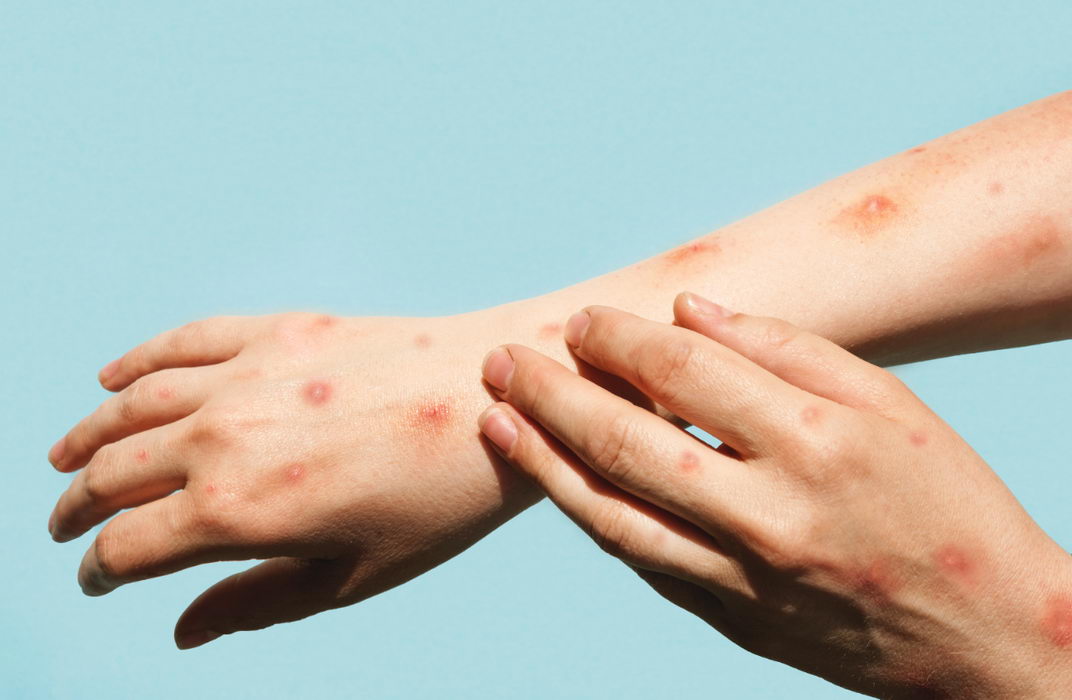
Figura 1: Lesiones de MPX.
La mayoría de los casos de MPX en humanos experimentan síntomas de leves a moderados. Complicaciones en países endémicos incluyen encefalitis, infecciones bacterianas cutáneas secundarias, deshidratación, conjuntivitis, queratitis y neumonía [5,11]. Las tasas de mortalidad publicadas varían sustancialmente y son vulnerables al sesgo de determinación de casos [12]. Se han informado tasas de letalidad que oscilan entre el 1 % y el 10 % en brotes en la cuenca del Congo, y el clado del virus que circula en esta región parece estar asociado con mayor virulencia [12-14]. El clado de África occidental, que es responsable de los brotes recientes en Nigeria, está asociado con una tasa de mortalidad general más baja consistentemente inferior al 3% [12,15]. Hasta la fecha, la mayoría de las muertes notificadas han ocurrido en niños pequeños y personas con VIH [12,15,16].
MPX no se propaga fácilmente entre las personas. Entre humanos, el virus puede transmitirse por vías respiratorias durante el contacto directo y prolongado cara a cara. Además, el MPX puede ser transmitido por contacto directo con fluidos corporales de una persona infectada, contacto de mucosas o piel no intacta con lesiones cutáneas abiertas o con objetos contaminados con virus, como ropa de cama o ropa [2,5]. La transmisión sexual de MPX se ha descrito en la literatura, pero con poca frecuencia. Ogoima et al. [17] planteó la hipótesis de que la transmisión sexual era una ruta plausible de infección, ya que implicaba contacto directo piel con piel, contacto durante las relaciones sexuales o transmisión a través de las secreciones genitales, al informar sobre el brote de MPX en humanos durante 2017 en Nigeria. La infección de parejas sexuales, tanto femeninas como masculinas, se ha informado previamente por el virus vaccinia, otro virus del género Orthopoxvirus, post vacunación contra la viruela [18,19].
MPX rara vez se exporta desde el continente africano. En 2003, hubo un brote zoonótico en EE. UU. que causó 47 casos confirmados o sospechosos [20-22]. Este brote estuvo relacionado con la importación de ratas gigantes, ardillas y lirones de Gambia, que habían transmitido el virus a los perritos de las praderas, que luego se vendían como mascotas. Solo 14 pacientes fueron hospitalizados y no hubo casos confirmados de transmisión de persona a persona. Se informaron infecciones importadas de viruela del simio en humanos después de un viaje en el Reino Unido [23], Israel [24], Singapur [25], y en 2021, en los EE. UU [20]
Recientemente, el 7 de mayo de 2022, el Reino Unido (UK) notificó un caso importado de MPX en una persona que viajaba desde Nigeria. A partir del 18 de mayo, varios Estados miembros de la UE/EEE informaron casos sospechosos o confirmados adicionales [26]. Hoy, la prevalencia de los casos de MPX continúa aumentando en todo el mundo, con un total de más de 16.500 casos globales confirmados hasta el 24 de julio de este año [27].
El tratamiento es principalmente sintomático y de apoyo (alivio de la fiebre y el prurito, hidratación), que incluye prevención y tratamiento de infecciones bacterianas secundarias. Los antivirales tecovirimat, brincidofovir y cidofovir son opciones potenciales para casos severos [5]. Solo Tecovirimat tiene autorización de comercialización en la UE para el tratamiento de infección por ortopoxvirus, incluido MPX. Actualmente existen datos limitados sobre eficacia y seguridad, mientras que los estudios clínicos están en curso en África [28].
La vacunación previa contra la viruela puede conferir protección cruzada contra MPX, que se estimó a partir de estudios anteriores a ser tan alto como 85% [2]. El efecto protector de la vacuna contra la viruela disminuye con el tiempo, aunque las serologías indican que puede durar más de 20 años. Sin embargo, se cree que a pesar del efecto menguante la vacuna contra la viruela confiere protección de por vida contra enfermedades graves debido a las células B y T de memoria [29]. Actualmente no hay ninguna vacuna autorizada en la UE contra MPX, pero la vacunación temprana posterior a la exposición (dentro de los cuatro días de la exposición a un caso de MPX) con la vacuna contra la viruela puede prevenir la enfermedad o hacer su curso menos grave [30,31]. Una vacuna contra la viruela no replicante de tercera generación (ImvanexTM - Modified Vaccinia Ankara) fue autorizada en circunstancias excepcionales por la EMA en 2013 para su uso contra la viruela [32]. Esta vacuna tiene indicación de uso en pacientes con infección por VIH para la viruela, pero actualmente no tiene autorización para su uso contra MPX [32]. Las vacunas contra la viruela de generaciones anteriores se han utilizado durante años (DryvaxTM y ACAM2000TM), sin embargo, están asociadas con efectos secundarios graves, incluidos efectos secundarios cardíacos, y ya no están autorizados en la UE.
Teniendo en cuenta todos estos factores y debido al aumento de casos, la Organización Mundial de la Salud ha declarado a la viruela símica como emergencia sanitaria mundial el 23 de julio instando a los gobiernos a tomar medidas coordinadas para detener la propagación del virus [33].
Referencias:
1. Durski KN, McCollum AM, Nakazawa Y, Petersen BW, Reynolds MG, Briand S, et al. (2018) Emergence of monkeypox— west and central Africa, 1970–2017. Morbidity and mortality weekly report. 67(10):306. https://www.cdc.gov/mmwr/volumes/67/wr/mm6710a5.htm
2. McCollum AM, Damon IK. (2014) Human monkeypox. Clinical Infectious Diseases. 58(2):260-7. https://academic.oup.com/cid/article-abstract/58/2/260/335791
3. Simpson K, Heymann D, Brown CS, Edmunds WJ, Elsgaard J, Fine P, et al. (20200 Human monkeypox–After 40 years, an unintended consequence of smallpox eradication. Vaccine 38(33):5077-81. https://www.sciencedirect.com/science/article/pii/S0264410X2030579X
4. Ladnyj I, Ziegler P, Kima E. (19720 A human infection caused by monkeypox virus in Basankusu Territory, Democratic Republic of the Congo. Bulletin of the World Health Organization. 46(5):593. https://www.ncbi.nlm.nih.gov/pmc/articles/PMC2480792/
5. World Health Organization (WHO). Monkeypox fact sheet. Geneva: WHO; 2019. https://www.who.int/news-room/fact-sheets/detail/monkeypox
6. Doty JB, Malekani JM, Kalemba LsN, Stanley WT, Monroe BP, Nakazawa YU, et al. (2017) Assessing monkeypox virus prevalence in small mammals at the human–animal interface in the Democratic Republic of the Congo. Viruses 9(10):283. Available at: https://www.mdpi.com/227974
7. Essbauer S, Meyer H. (2007) Genus Orthopoxvirus: Monkeypox virus. In: Poxviruses. Basel, Switzerland: Birkhäuser.
8. Learned LA, Reynolds MG, Wassa DW, Li Y, Olson VA, Karem K, et al. (2005) Extended interhuman transmission of monkeypox in a hospital community in the Republic of the Congo, 2003. The American Journal of Tropical Medicine and Hygiene. 73(2):428-34. https://www.ajtmh.org/view/journals/tpmd/73/2/article-p428.xml
9. Nolen LD, Osadebe L, Katomba J, Likofata J, Mukadi D, Monroe B, et al. (2016) Extended human-to-human transmission during a monkeypox outbreak in the Democratic Republic of the Congo. Emerging infectious diseases. 22(6):1014. https://www.ncbi.nlm.nih.gov/pmc/articles/pmc4880088/
10. MacNeil A, Reynolds MG, Braden Z, Carroll DS, Bostik V, Karem K, et al. (2009) Transmission of atypical varicella-zoster virus infections involving palm and sole manifestations in an area with monkeypox endemicity. Clinical Infectious Diseases. 48(1):e6-e8. https://academic.oup.com/cid/articleabstract/48/1/e6/291721
11. Huhn GD, Bauer AM, Yorita K, et al. (2005) Clinical characteristics of human monkeypox, and risk factors for severe disease. Clin Infect Dis 41: 1742–51.
12. Beer EM, Rao VB. (2019) A systematic review of the epidemiology of human monkeypox outbreaks and implications for outbreak strategy. PLoS Negl Trop Dis 13: e0007791.
13. Jezek Z, Grab B, Szczeniowski M, Paluku KM, Mutombo M. (1988) Clinicoepidemiological features of monkeypox patients with an animal or human source of infection. Bull World Health Organ 66: 459–64
14. Likos AM, Sammons SA, Olson VA, et al. (2005) A tale of two clades: monkeypox viruses. J Gen Virol 86: 2661–72.
15. Yinka-Ogunleye A, Aruna O, Dalhat M, et al. (2019) Outbreak of human monkeypox in Nigeria in 2017–18: a clinical and epidemiological report. Lancet Infect Dis 19: 872–79.
16. Ogoina D, Iroezindu M, James HI, et al. (2020) Clinical course and outcome of human monkeypox in Nigeria. Clin Infect Dis 71: e210–14.
17. Ogoina D, Izibewule JH, Ogunleye A, Ederiane E, Anebonam U, Neni A, et al. (2019) The 2017 human monkeypox outbreak in Nigeria—report of outbreak experience and response in the Niger Delta University Teaching Hospital, Bayelsa State, Nigeria. PLoS One. 14(4):e0214229. https://journals.plos.org/plosone/article?id=10.1371/journal.pone.0214229
18. Shao H, McDonald EC, Ginsberg MM, Yee LM, Montgomery JR, Allan-Martinez F, et al. (2010) Vaccinia virus infection after sexual contact with a military smallpox vaccinee-Washington, 2010. MMWR Morbidity and Mortality Weekly Report. 59(25):773-5. https://www.cdc.gov/mmwr/preview/mmwrhtml/mm5925a2.htm
19. McLaughlin J, Schmidt T, Westcott M, Baumbach J, Lofgren J, Gerber S, et al. (2007) Vulvar vaccinia infection after sexual contact with a military smallpox vaccinee--Alaska, 2006. MMWR Morbidity and mortality weekly report 56(17):417-9. https://jamanetwork.com/journals/jama/fullarticle/207576
20. CDC. Monkeypox in the United States. 2021. https://www.cdc.gov/ poxvirus/monkeypox/outbreak/us-outbreaks.html , accesado 14/03/2022.
21. Reed KD, Melski JW, Graham MB, et al. (2004) The detection of monkeypox in humans in the western hemisphere. N Engl J Med 350: 342–50.
22. Reynolds MG, Yorita KL, Kuehnert MJ, et al. (2006) Clinical manifestations of human monkeypox influenced by route of infection. J Infect Dis 194: 773–80
23. Vaughan A, Aarons E, Astbury J, et al. (2018) Two cases of monkeypox imported to the United Kingdom, September 2018. Euro Surveill 23: 1800509.
24. Erez N, Achdout H, Milrot E, et al. (2029) Diagnosis of imported monkeypox, Israel, 2018. Emerg Infect Dis 25: 980–83.
25. Ng OT, Lee V, Marimuthu K, et al. (2019) A case of imported monkeypox in Singapore. Lancet Infect Dis 19: 1166.
26. Monkeypox multi-country outbreak 23 May 2022 ECDC
27. The Program for Monitoring Emerging Diseases (ProMED) https://promedmail.org/
28. European Medicines Agency (EMA). Tecovirimat SIGA. Amsterdam: EMA; 2022. https://www.ema.europa.eu/en/medicines/human/EPAR/tecovirimat-siga
29. Kunasekaran MP, Chen X, Costantino V, Chughtai AA, MacIntyre CR. (2019) Evidence for residual immunity to smallpox after vaccination and implications for re-emergence. Military Medicine 184(11-12):e668-e79. https://academic.oup.com/milmed/article-abstract/184/11-12/e668/5542515
30. Centers for Disease Control and Prevention (CDC). Monkeypox - Treatment. Atlanta: CDC; 2021. http://www.cdc.gov/poxvirus/monkeypox/treatment.html
31. European Centre for Disease Prevention and Control (ECDC). Factsheet for health professionals on monkeypox. Stockholm: ECDC; 2019. https://www.ecdc.europa.eu/en/all-topics-z/monkeypox/factsheet-healthprofessionals
32. European Medicines Agency (EMA). Imvanex - Smallpox vaccine (Live Modified Vaccinia Virus Ankara) -Authorisation details. London: EMA; 2013. https://www.ema.europa.eu/en/medicines/human/EPAR/imvanex#authorisation-details-section
33. Organización Panamericana de la Salud. https://www.paho.org/es/noticias/23-7-2022-director-general-oms-declaro-que-brote-viruela-simica-constituye-emergencia , accesado 26/07/2022.
 ISSN 1666-7948 www.quimicaviva.qb.fcen.uba.ar |
Revista QuímicaViva Volumen 21, Número 2, Agosto de 2022 |
Publicado en:
Vol 21, Nro 2
Agosto de 2022
Identificador: E0235
DOI:No disponible
Tipo: Revisiones
Contacto: Carlos Alberto Bueno