
ISSN 1666-7948
Revista Electrónica de Ciencia y Educación
Departamento de Química Biológica FCEN-UBA IQUIBICEN

ISSN 1666-7948
Revista Electrónica de Ciencia y Educación
Departamento de Química Biológica FCEN-UBA IQUIBICEN
Derivados de sales de arildiazonio
Miguel Morales Toyo
Facultad de Ciencias y Humanidades, Escuela de Educación, Universidad Central del Este (UCE), Avenida Francisco Alberto Caamaño Deñó, San Pedro de Macorís, República Dominicana.
Laboratorio de Electrónica Molecular (LEM), Departamento de Química, Facultad Experimental de Ciencias, La Universidad del Zulia, Ap. 526, Grano de Oro, Módulo No.
2, Maracaibo, Estado Zulia, República Bolivariana de Venezuela.
Resumen
Las sales de arildiazonio son compuestos altamente reactivos que pueden obtenerse a través de diferentes metodologías, estas sales han sido ampliamente utilizadas como intermediarios claves para la preparación de muchos compuestos de importancia industrial y farmacéutica, un ejemplo de ello, elresveratrol. En este sentido presentaremos una breve descripción de diferentes técnicas y tipos de reacciones para la obtención de sales de arildiazonio como intermediarios para la síntesis de diversos derivados.
Palabras clave: Derivados, sales de arildiazonio, reacciones, síntesis.
Derivatives of Aryldiazonium salts
Summary
Aryldiazonium salts are highly reactive compounds that can be obtained through different methodologies, these salts have been widely used as key intermediates for the preparation of many compounds of industrial and pharmaceutical importance, as is the case of resveratrol. In this sense, we will present a brief description of different techniques and reaction types for obtaining aryldiazonium salts as intermediates for the synthesis of several derivatives.
Keywords: Derivatives, aryldiazonium salts, reactions, synthesis.
Introducción
Cuando una amina primaria aromática es tratada con ácido nitroso en una solución fría se obtieneun compuesto intermediario inestable denominado sal de arildiazonio (ArN2+), esta clase de intermediario ha sido utilizadaprincipalmente para la síntesis de colorantes o azo compuestos [1]. Sin embargo, sus aplicaciones se han extendido como sustratos o intermediarios para diferentes reacciones que van desde sus reducciones hasta acoplamientos cruzados, y más recientemente se han empleado para la modificación de superficies de biopolímeros, nanomateriales, resinas, así como para la obtención de nuevos materialesy su aplicación como sensores por citar algunos ejemplos.[2–4,5] A continuación describiremos la preparación de sales de arildiazonio, así como los métodos empleados en las que dichas sales han sido utilizadas como intermediarios de síntesis.
Métodos de preparación de sales de arildiazonio
El método más común para la preparación de sales de diazonio es la generación in situ de ácidonitroso, HNO2, que se obtiene al hacer reaccionar una amina clorhidrato con NaNO2 (1) en medio acuoso y a bajas temperaturas (alrededor de los 0°C); para el caso en que las sales de arildiazonio presentan baja solubilidad en medio acuoso, estas pueden prepararse con ácido nitrosilsulfúrico (HSO4NO)(2), este último se obtiene al mezclar H2SO4 con NaNO2 el procedimiento se lleva a cabo con previa disolución de la amina en H2SO4y posterior adición de NaNO2.[1, 2, 6–8] Las sales de arildiazonio también pueden prepararse bajo la forma de tetraflouroboratos (3), empleando BF3, OEt2 y tert-BuONO, por citar algunos ejemplos.[3]
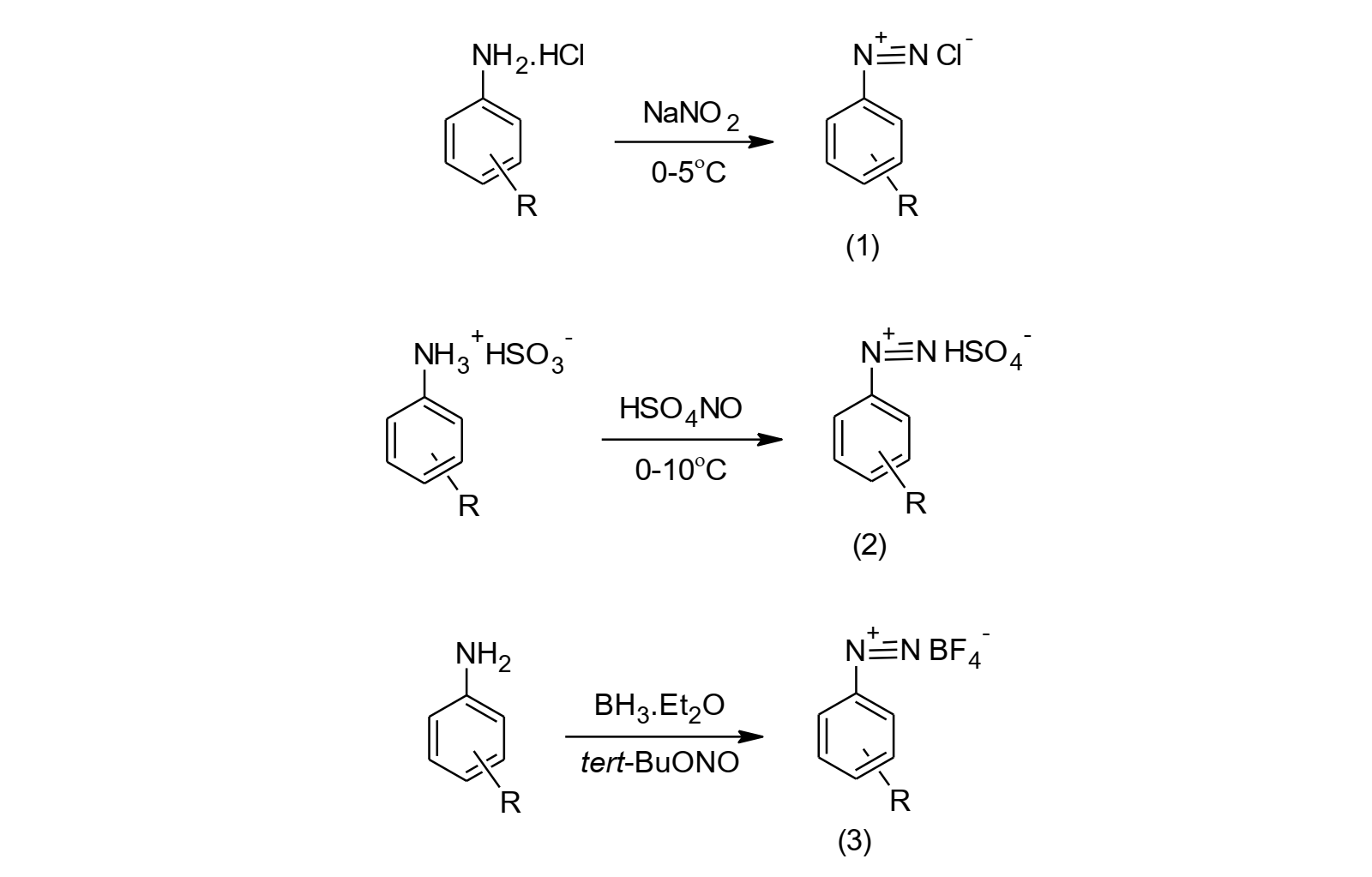
Figura 1: Síntesis de sales de diazonio.
Reducción
Las sales de arildiazonio pueden reducirse en presencia de H2SO3(ac) o Na2SO3 para generar las correspondientessulfonas (4), que posteriormente son hidrolizadas con HCl concentrado y así obtenerlos respectivosclorhidratosde fenilhidracina (5). El H2SO3 es generado in situ cuando sesatura agua a 0-5°C con SO2.[6, 7].
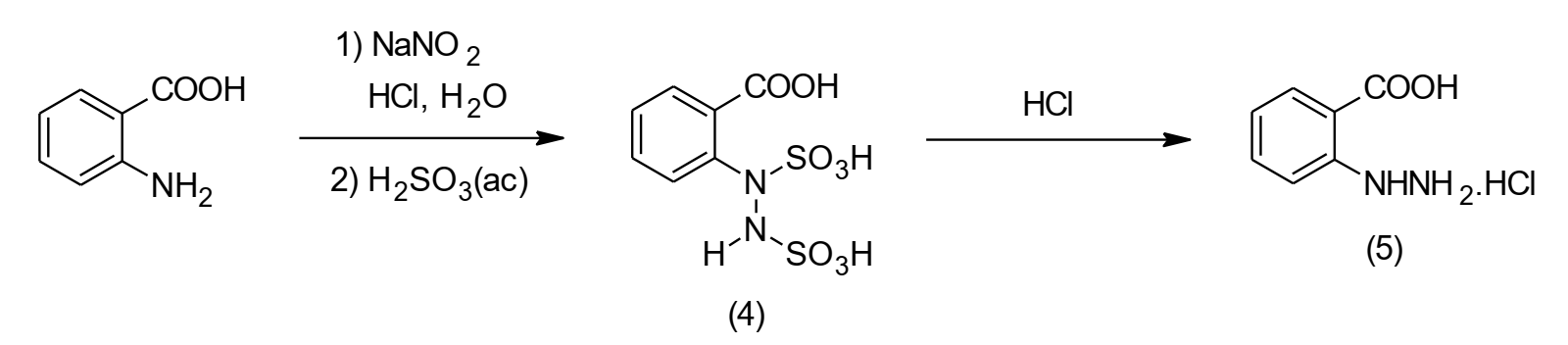
Figura 2: Reducción de sales de diazonio para la obtención de derivados de fenilhidracina clorhidrato.
Nuestro grupo de investigación está particularmente interesado en la obtención de derivados de clorhidratos de fenilhidracinapara ser empleados como intermediarios en la síntesis de derivados de fenilhidrazonas, compuestos que presentan un amplio espectro de actividades biológicas.[9–12]
Sustitución Nucleofílica
Ambroise y col. utilizaron como intermediario de reacción a la sal de diazonio delp-aminofenil-α-D-galactopiranosa empleando ácido trifluoracético para generar el ácido nitroso (6). Posteriormente llevaron a cabo la sustitución nucleofílica del grupo azo por una azida, utilizando NaN3 como agente nucleófilico a temperatura ambiente, el p-azidofenil-α-D-galactopiranosa (7) se obtuvo con un rendimiento del 77 %.[13, 14]
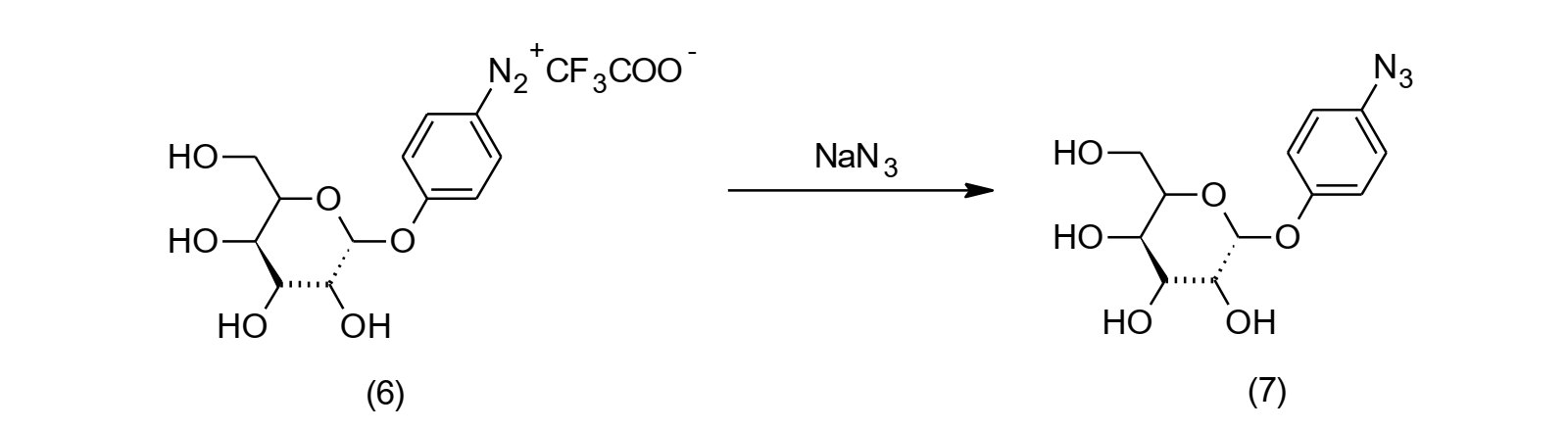
Figura 3: Reacción de sustitución nucleofílica de un grupo azo.
Arilación de Meerwein
Karminski-Zamola y col., sintetizaron una serie de derivados de arilfuranos y ariltiofenos (8) a través del acoplamiento de la sal del p-carboxi arenodiazonio (9) y sustratos de furano y tiofeno (10) en presencia de CuCl2x2H2O. Todo esto para ser empleados como intermediarios para la obtención de derivados de tipo bis-Benzotiazolil [15].
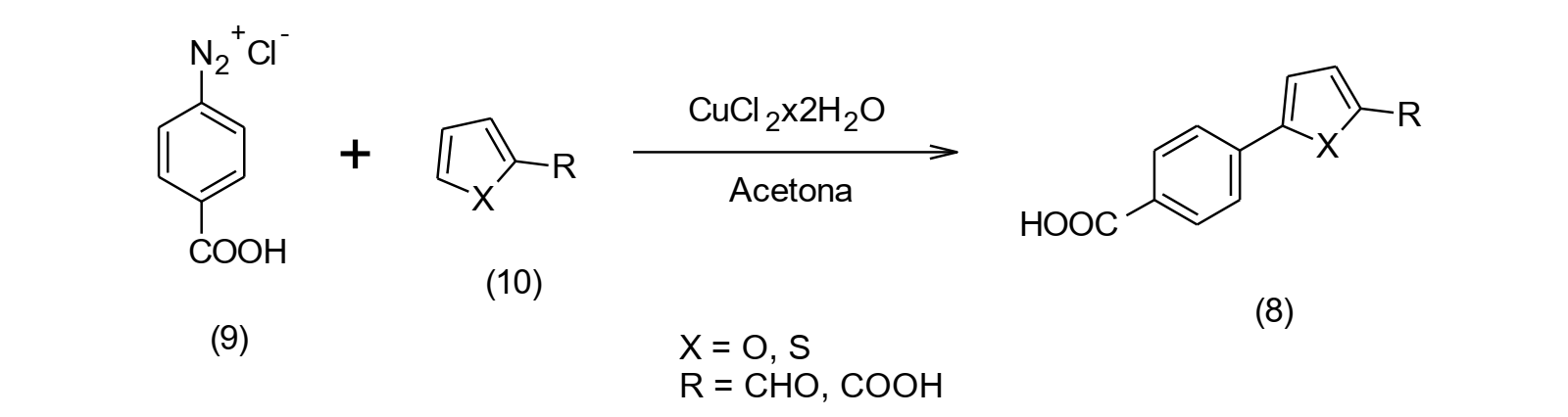
Figura 4: Síntesis de derivados de arilfuranos y ariltiofenos.
Acoplamientos
Darwish y col., encontraron que al acoplar la base nitrogenenada 2-(bencilsulfanil)-7H-purin-6-ona (11) con diferentes sales de arildiazonio se obtienen compuestos 8-arilhidrazono con rendimientos moderados (30-65%) y en forma de tautómeros, también determinaron espectroscópicamente que los isómero arilhidrazona (12) son las especies que predomina frente a los azo (13) en dichos equilibrios tautoméricos [16].
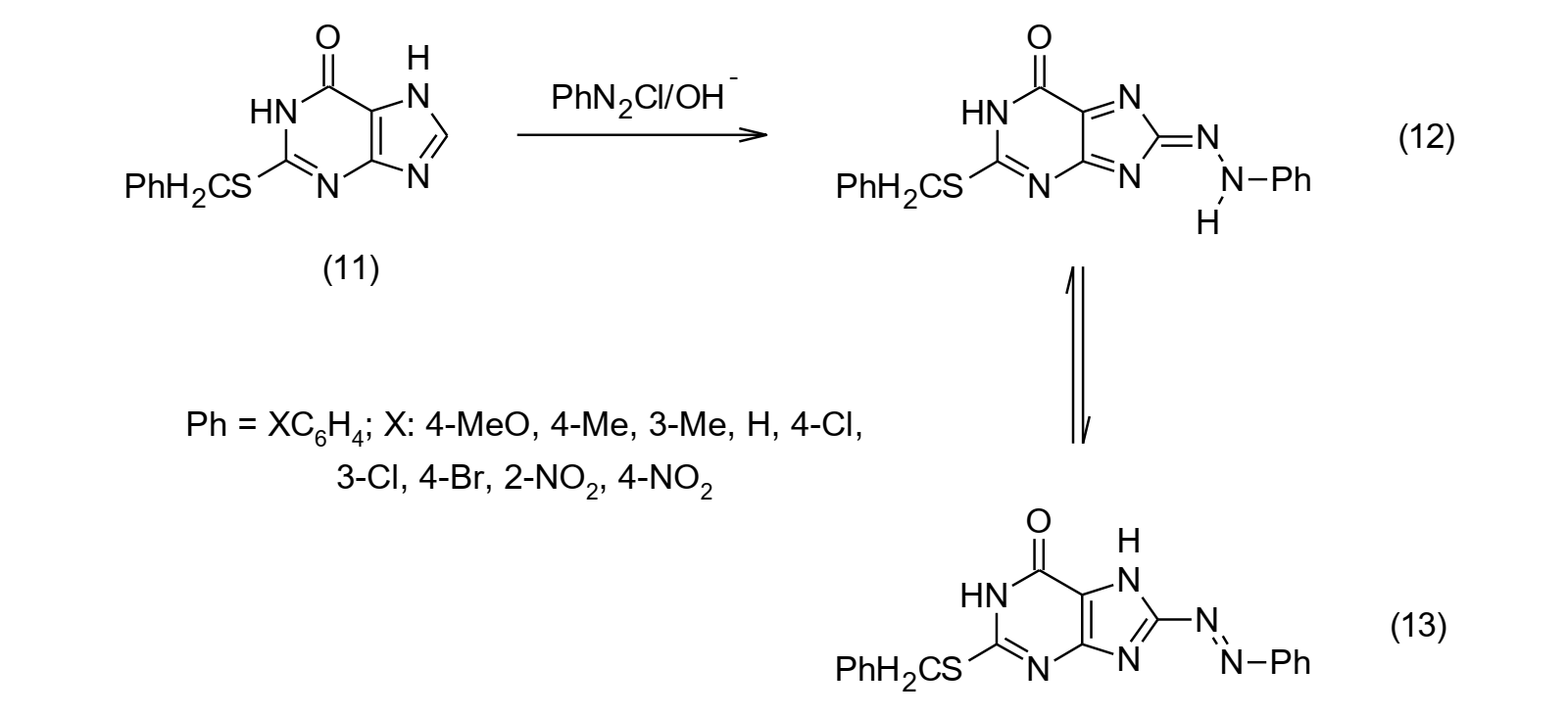
Figura 5: Acoplamientos de sales de arildiazonio con bases nitrogenadas.
Acoplamientos con metilenos activos
Los azo compuestos son colorantes sintéticos de mucha importancia, sin embargo esta clase de compuesto son considerados potenciales carcinógenos. Por otro lado, los colorantes hidrazona son considerados no mutagénicos y no genotóxicos, en este sentido Rollas y col., reportaron el acoplamiento del N-(2,4-dimetilfenil)-3-oxobutamida (14) que posee un grupo metileno activo con diferentes sales de diazonio en presencia de acetato de sodio.[17–19]
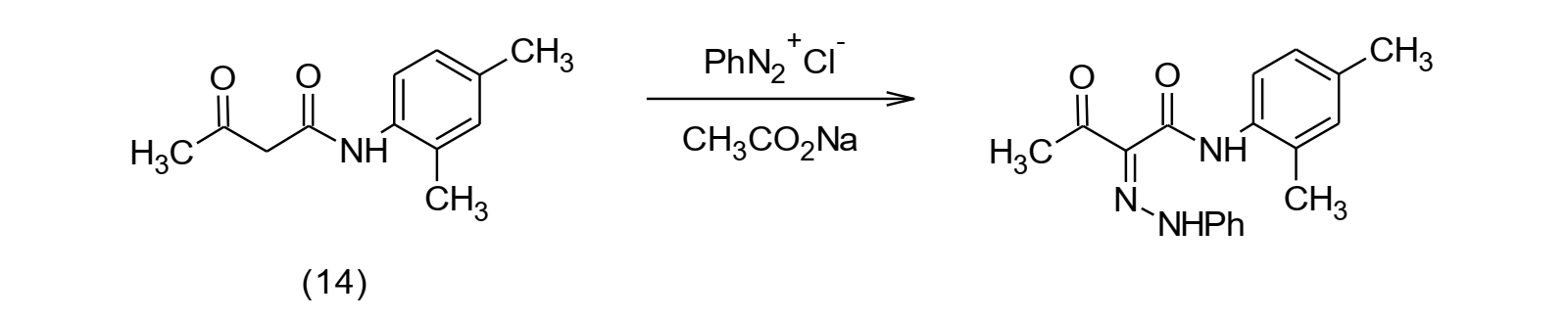
Figura 6: Acoplamientos de sales de arildiazonio con metilenos activos.
Arilación de Heck-Matsuda
Correira y col., llevaron a cabo la síntesis regio y estereoselectiva del trans-3,5-dimetoxi-4´-acetoxi-estilbeno (15) evidencia del isómero cis como intermediario para la síntesis del agente anticáncer resveratrol en alto rendimiento, al acoplar 3,4-dimetoxibencenodiazonio tetrafluoroborato (16) con el 4-acetoxi-estireno (17), catalizada con un 4 mol % de Pd(OAc)2 en atmosfera de CO [20, 21].
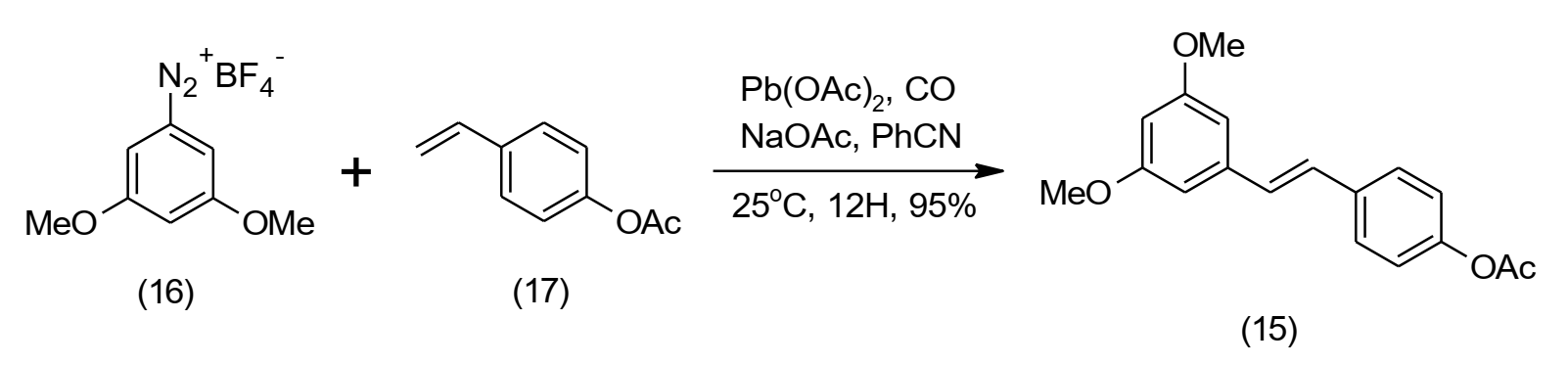
Figura 7: Síntesis de trans-estilbenos.
Arilación Reductiva
Esta es una modificación de la reacción de Arilación de Meerwein en el que no se requieren metales de transición para el proceso de Arilación y reducción para la obtención de α-arilacetonas (18) utilizando sales de tetrafluoroborato de diazonio (19) y acetato de isoprenilo. Esta clase de compuestos pueden obtenerse a gran escala, en buenos rendimientos y empleando reactivos de bajo costo y de baja toxicidad [22].
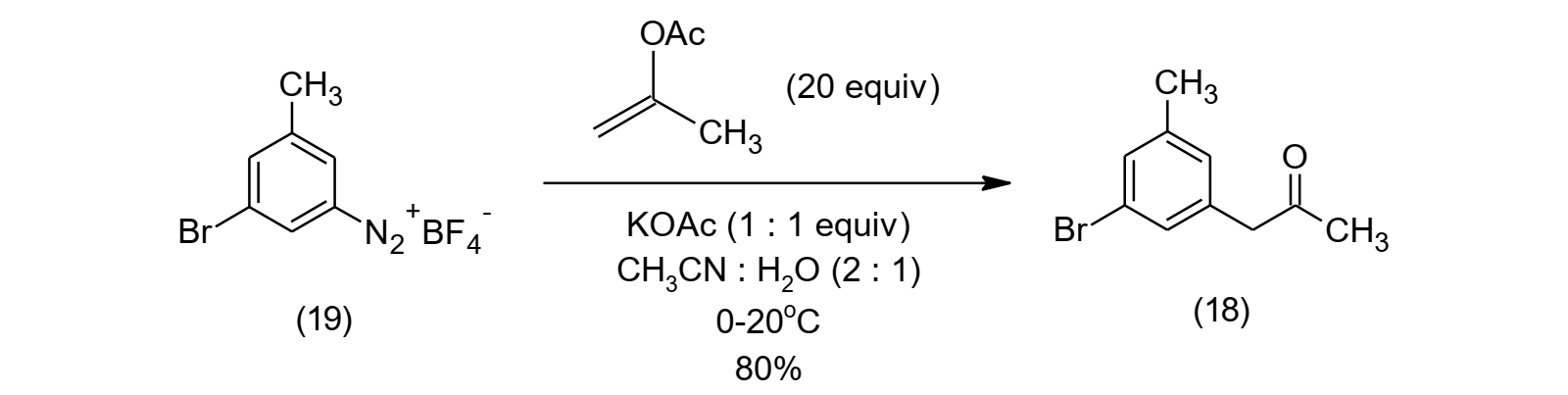
Figura 8: Síntesis de α-arilacetonas por arilación reductiva de sales de arildiazonio.
Conclusiones
La presencia del grupo diazo en las sales de arildiazonio los hace sensibles a los reactivos nucleófilos, reaccionando con ellos generalmente de manera fácil debido a su alta reactividad. Esta propiedad útil implica que las sales de arildiazonio son valiosas como "componentes básicos" en la síntesis de una amplia gama de compuestos, tales como colorantes y fármacos con propiedades biológicas como el anticancerígeno. Por lo tanto, la síntesis de nuevos derivados de sales de arildiazonio es muy necesaria y puede traer el descubrimiento de nuevas sustancias con propiedades interesantes.
Referencias:
1. Tuuttila T, Lipsonen J, Huuskonen J, and Rissanen K. (2009) Chiral donor-π-acceptor azobenzene dyes. Dye Pigment 80: 34–40 DOI: 10.1016/j.dyepig.2008.04.007.
2. Roglans A, Pla-Quintana A, and Moreno-Mañas M. (2006) Diazonium salts as substrates in palladium-catalyzed cross-coupling reactions. Chemical Reviews 106: 4622–4643 DOI: 10.1021/cr0509861.
3. Schroen M, and Bräse S. (2005) Polymer-bound diazonium salts for the synthesis of diazoacetic esters. Tetrahedron 61: 12186–12192 DOI: 10.1016/j.tet.2005.09.145.
4. Radulescu MC, Chira A, Radulescu M, Bucur B, Bucur MP, and Radu GL. (2010) Determination of silver(I) by differential pulse voltammetry using a glassy carbon electrode modified with synthesized N-(2-aminoethyl)-4,4’-bipyridine. Sensors 10: 11340–11351 DOI: 10.3390/s101211340.
5. Mahouche-Chergui S, Gam-Derouich S, Mangeney C, and Chehimi MM. (2011) Aryl diazonium salts: a new class of coupling agents for bonding polymers, biomacromolecules and nanoparticles to surfaces. Chemical Society Reviews 40: 4143 DOI: 10.1039/c0cs00179a.
6. Stephenson E. (1949) Indazole. Organic Synththesis 29: 54 DOI: 10.15227/orgsyn.029.0054.
7. Coleman G. (1922) Phenylhydrazine. Organic Syntheses 2: 71 DOI: 10.15227/orgsyn.002.0071.
8. Naik SJ, and Halkar UP. (2005) Synthesis and application of novel 4,5,6,7-tetrahydrobenzothiazole based azo disperse dyes. Arkivoc 2005: 141–149 DOI: http://dx.doi.org/10.3998/ark.5550190.0006.d12.
9. Restrepo J, Glidewell C, Cubillán N, Alvarado Y, Dege N, and Morales-Toyo M. (2019) Synthesis, crystal structure, and non-covalent interactions in ethyl 4-hydrazinobenzoate hydrochloride. Journal of Molecular Structure 1177: 363–370 DOI: 10.1016/j.molstruc.2018.09.056.
10. Morales-Toyo M, Cubillán N, Glidewell C, Seijas L, Boscan-Melean K, and Restrepo J. (2019) Synthesis, crystal structure, and non-covalent interactions in 4-hydrazinobenzoic acid hydrochloride. Journal of Moecular l. Structure DOI: https://doi.org/10.1016/j.molstruc.2019.127154.
11. Morales-Toyo M, Alvarado YJ, Restrepo J, Seijas L, Atencio R, and Bruno-Colmenarez J. (2013) Synthesis, Crystal Structure Analysis, Small Cluster Geometries and Energy Study of (E)-Ethyl-4-(2-(thiofen-2-ylmethylene)hydrazinyl)benzoate. Journal Chemical Crystallography 43: 544–549 DOI: 10.1007/s10870-013-0455-5.
12. Morales-Toyo M, Glidewell C, Bruno-Colmenares J, Cubillán N, Sánchez-Colls R, Alvarado Y, et al. (2019) Synthesis of (E)-Ethyl-4-(2-(furan-2-ylmethylene)hydrazinyl)benzoate, crystal structure, and studies of its interactions with human serum albumin by spectroscopic fluorescence and molecular docking methods. Spectrochimica Acta Part A Molecular and Biomolecular Spectroscopy 216: 375–384 DOI: 10.1016/j.saa.2019.03.028.
13. Ambroise Y, Mioskowski C, Leblanc G, and Rousseau B. (2000) Syntheses and properties of photoactivatable sugar derivatives designed to probe the sugar-binding site of melibiose permease. Bioorganic Medicinal Chemistry Letters 10: 1125–1127 DOI: 10.1016/S0960-894X(00)00180-3.
14. Teimouri A, Chermahini AN, and Emami M. (2008) Synthesis , spectroscopic characterization and DFT calculations on. 2008: 172–187 DOI: http://dx.doi.org/10.3998/ark.5550190.0009.c19.
15. Racanè L, Tralić-Kulenović V, Boykin DW, and Karminski-Zamola G. (2003) Synthesis of new cyano-substituted bis-benzothiazolyl arylfurans and arylthiophenes. Molecules 8: 342–349 DOI: 10.3390/80300342.
16. Darwish ES, Mosselhi MA, Altalbawy FM, and Saad HA. (2011) Synthesis, acidity constants and tautomeric structure of the diazonium coupling products of 2-(benzylsulfanyl)-7H-purin-6-one in its ground and excited states. Molecules 16: 8788–8802 DOI: 10.3390/molecules16108788.
17. Ça M, Rollas S, Küçükgüzel ŞG, and Koçyi B. (2008) Synthesis and structure elucidation of hydrazones derived from N - ( 2 , 4-dimethylphenyl ) -3-oxobutanamide. Arkivoc 2008: 188–194 DOI: http://dx.doi.org/10.3998/ark.5550190.0009.c20.
18. Rollas S, and Küçükgüzel ŞG. (2007) Biological activities of hydrazone derivatives. Molecules 12: 1910–1939 DOI: 10.3390/12081910.
19. Mohamed A. Saleh, Mohamed F. Abdel-Megeed, Mohamed A. Abdo A-BMS. (2003) Molecules 2003 , 8 , 363-373. 8: 363–373 DOI: 10.3390/80400363.
20. Moro AV, Cardoso FSP, and Correia CRD. (2008) Heck arylation of styrenes with arenediazonium salts: short, efficient, and stereoselective synthesis of resveratrol, DMU-212, and analogues. Tetrahedron Letters. 49: 5668–5671 DOI: 10.1016/j.tetlet.2008.07.087.
21. Taylor JG, and Correia CRD. (2011) Stereoselective Synthesis of Unsymmetrical β,β-Diarylacrylates by a Heck-Matsuda Reaction: Versatile Building Blocks for Asymmetric Synthesis of β,β-Diphenylpropanoates, 3-Aryl-indole, and 4-Aryl-3,4-dihydro-quinolin-2-one and Formal Synthesis of (-)-Inda. Journal of Organic Chemistry 76: 857–869 DOI: 10.1021/jo102134v.
22. Molinaro C, Mowat J, Gosselin F, O’Shea PD, Marcoux J-F, Angelaud R, et al. (2007) A practical synthesis of alpha-aryl methyl ketones via a transition-metal-free Meerwein arylation. Journal of Organic Chemistry 72: 1856–1858 DOI: 10.1021/jo062483g.
 ISSN 1666-7948 www.quimicaviva.qb.fcen.uba.ar |
Revista QuímicaViva Volumen 19, Número 2, Agosto de 2020 |
Publicado en:
Vol 19, Nro 2
Agosto de 2020
Identificador: E0167
DOI:No disponible
Tipo: Trabajos de investigación
Recibido en: 07/10/2019
Aceptado en: 11/03/2020
Contacto: Miguel Morales Toyo