|
|
Revista QuímicaViva Número 3, año 3, septiembre 2004 quimicaviva@qb.fcen.uba.ar |
Ontogenia B: el delicado equilibrio entre la diversidad y la
autoinmunidad
Romina Gamberale*
Laboratorio de Inmunología, IIHema, Academia
Nacional de Medicina
Recibido 10 de agosto de 2004
Aceptado 29 de agosto de 2004
Resumen
Los linfocitos B, al igual que el
resto de las células del sistema inmune, se originan en médula ósea a partir de
un precursor común. Las células B comienzan su maduración en la médula ósea y
la finalizan en el bazo. Durante las primeras etapas de desarrollo, los
esfuerzos se centran en la generación de la inmunoglobulina de superficie que
es parte del receptor B (BCR). Una vez que el BCR puede ser expresado en la
membrana, los mecanismos de control evalúan la especificidad del mismo,
eliminando a aquellos linfocitos B cuyos BCR reconozcan moléculas propias. Si
bien durante la ontogenia de linfocitos B la mayoría de las células muere por
apoptosis antes de alcanzar la madurez, este proceso, lejos de ser un gasto
innecesario de energía, mantiene el delicado equilibrio entre la diversidad y
la autoinmunidad.
Palabras
clave: linfocitos B, ontogenia
Ontogeny of B
lymphocytes: The subtle balance between diversity and autoimmunity"
Abstract
B lymphocytes, as other cells of the immune system, arise from
hematopoietic stem cells in the bone marrow. B cells mostly develop in the bone
marrow and complete their maturation in the spleen. During the early stages of
B cell development control mechanisms are focused on the generation of the
surface immunoglobulin, which is part of the BCR. Once the cell can express
this receptor the focus shifts to its specificity, eliminating those B
lymphocytes with self-reactive BCRs. During B cell development, most of the
cells die before become mature. This process, far from being an unnecessary
waste of energy, maintains the subtle balance between diversity and
autoimmunity.
Key words: B lymphocytes, ontogeny
Introducción
Los seres
humanos nos encontramos expuestos continuamente a una gran cantidad de
microorganismos potencialmente patógenos, sin embargo, sólo nos enfermamos en
forma ocasional. Esto es así gracias a nuestro sistema inmune, el cual
constituye un sistema muy eficiente de defensa contra la infección. Distintos
tipos de células sanguíneas tales como, neutrófilos, basófilos, eosinófilos,
monocitos/macrófagos, linfocitos T y linfocitos B, participan en la respuesta inmunológica. La
estrategia de defensa contra la infección involucra distintas etapas: una etapa temprana, conocida con
el nombre de inmunidad innata, y una etapa tardía denominada inmunidad
adaptativa.
Los linfocitos
B y T son los principales protagonistas de la respuesta inmune adaptativa y, a
diferencia del resto de las células del sistema inmune, poseen
en su membrana receptores antigénicos capaces de reconocer en forma específica
pequeñas porciones del patógeno (para el caso de los linfocitos B) o células
infectadas con los mismos (en el caso de los linfocitos T). Luego de este
reconocimiento, pueden activarse, multiplicarse y diferenciarse en células
efectoras capaces de defendernos contra ese microorganismo en particular. La estrategia
utilizada en la inmunidad adaptativa para reconocer a la gran cantidad de
microorganismos existentes, involucra a una inmensa variedad de linfocitos B y
T, cada uno de los cuales porta en su superficie un receptor particular para el
antígeno. Gracias a esta gran diversidad de receptores antigénicos, un
individuo tiene la capacidad de desarrollar
una respuesta inmune adaptativa contra la amplísima variedad
de patógenos con los que puede encontrarse durante su vida.
En este
artículo, veremos:
v
Las características del receptor
antigénico de los linfocitos B.
v
Las etapas de maduración de los
linfocitos B durante su desarrollo.
v
Cómo es posible generar la gran
diversidad de receptores antigénicos existentes.
¿Cómo es el receptor antigénico de los linfocitos B?
El receptor
antigénico de los linfocitos B se denomina BCR (B cell receptor) y está constituido por una inmunoglobulina (Ig)
asociada con un heterodímero formado por las moléculas Iga e Igb (Figura 1). La Ig que forma parte del BCR
no es otra cosa que una molécula de anticuerpo anclada a la membrana. Mientras
que esta molécula es la responsable del reconocimiento antigénico, la
transducción de la señal al interior de la célula B se lleva a cabo por el
heterodímero Iga-Igb.
|
|
Figura 1: El BCR está constituido por una
inmunoglobulina (Ig) de superficie y el heterodímero Iga-Igb. La Ig esta constituida por dos cadenas pesadas (H)
idénticas entre si, asociadas por puentes disulfuro y dos cadenas livianas (L)
idénticas entre si, asociadas a las H por puentes disulfuro. Comparando un gran
número de Ig, se observó que la porción amino-terminal de ambas cadenas es
variable (V) y está involucrada en el reconocimiento del antígeno. Por el
contrario, la porción carboxi-terminal de ambas cadenas es relativamente
constante (C). En la
figura se observan las cadenas H en color verde, las cadenas L en color
amarillo y los dominios variables rayados.
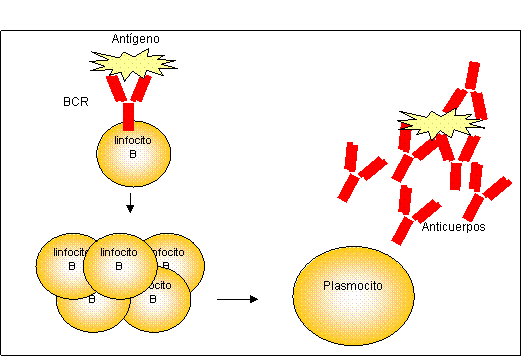
¿Qué función cumplen los linfocitos B?
Aquellos
linfocitos B que reconocen al antígeno específico a través del BCR, pueden
activarse y proliferar originando un clon de células hijas, para diferenciarse
posteriormente a plasmocitos (Figura 2). Estos últimos tienen la
capacidad de secretar moléculas de Ig (anticuerpos), los cuales poseen la misma
especificidad de la Ig que formaba parte inicialmente del BCR. Por lo tanto,
los anticuerpos secretados podrán reconocer al microorganismo y reclutar una
variedad de mecanismos efectores a fin de destruirlo.
|
|
Figura 2
Las
distintas porciones constantes de la cadena pesada (CH) dan origen a los
diferentes tipos de anticuerpos conocidos (IgM, IgG, IgE, IgA e IgD), y cada
una de estas clases de Ig es particularmente eficiente en la activación de los
distintos mecanismos efectores. Sin embargo, la Ig que forma parte del BCR no
lleva a cabo esas funciones ya que se encuentra anclada en la membrana de la
célula B, por lo tanto, solamente es capaz de reconocer al antígeno específico
a través de la región variable.
ONTOGENIA de LINFOCITOS B
¿Dónde se originan los linfocitos B?
Los
linfocitos B, al igual que el resto de las células del sistema inmune, se
originan en la médula ósea a partir de un precursor común, denominado stem cell o célula madre pluripotente hematopoyética (CMPH) (Figura 3).
Dichas células tienen la capacidad de autorrenovarse y son, tal como su nombre
lo indica, potencialmente capaces de dar lugar a distintos tipos celulares. En
el hombre, las CMPH aparecen en el saco vitelino embrionario alrededor de la
tercera semana de vida y, a medida que el feto se desarrolla, algunas de estas
células migran al hígado. Recién al cuarto mes de vida fetal la médula ósea
comienza a ser el sitio donde mayoritariamente ocurrirá la hematopoyesis. Si
bien en los adultos la mayor cantidad de CMPH se encuentra en la médula ósea, estas
células tienen la capacidad de migrar hacia la circulación, por lo que puede
hallarse una pequeña proporción en sangre periférica.
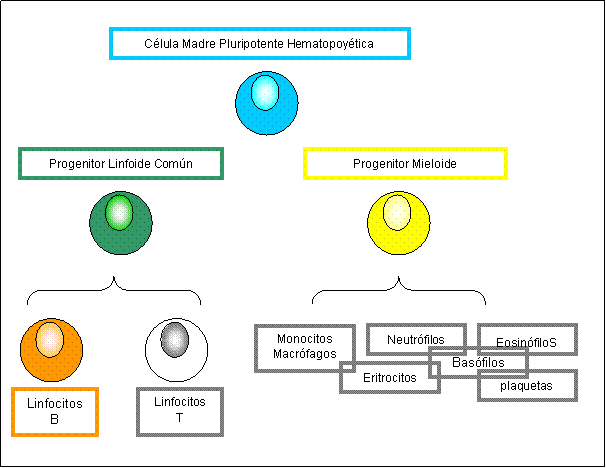
A partir de
las CMPH se generan dos tipos de progenitores con potencial pluripotente más
acotado que se denominan: progenitor
mieloide, el cual podrá diferenciarse en células de estirpe mieloide
(eritrocitos, plaquetas, monocitos y granulocitos neutrófilos, basófilos y
eosinófilos) y progenitor linfoide común (PLC), a partir del cual se
generarán los linfocitos B y T. ¿Cómo se decide si el PLC se diferenciará hacia
el linaje B ó T? Hasta el momento no está del todo claro este punto, sin
embargo, numerosas evidencias sugieren que la señalización a través de una
molécula presente en la membrana de los PLC, denominada Notch1, induciría la
diferenciación hacia el linaje T, mientras que la ausencia ó inhibición de esa
señal favorecería la diferenciación B.
|
|
Figura 3
¿Dónde se desarrollan los linfocitos B?
Los
linfocitos B se desarrollan mayoritariamente en la médula ósea pero culminan su
maduración en el bazo. Su generación se produce en distintas etapas o pasos que
deben ir completándose, uno a uno, en forma correcta para poder avanzar en el
proceso de maduración. El concepto mismo de maduración linfocitaria implica la
generación de un receptor antigénico particular para cada linfocito y su
expresión en la membrana antes del ingreso del antígeno. Dado que existen miles
de millones de linfocitos B distintos, cada uno de los cuales porta
inmunoglobulinas de superficie con una especificidad única, un individuo posee
una gran diversidad de inmunoglobulinas. Tal como veremos a continuación, en
las primeras etapas del desarrollo linfocitario, los esfuerzos se centran en la
generación de esta Ig y, si esto no es posible, el linfocito no continúa con su
desarrollo y se ponen en marcha mecanismos que llevan a la muerte celular
programada conocida como apoptosis,
sin alcanzar la madurez.
¿Cómo es posible generar tanta diversidad de inmunoglobulinas?
Las
inmunoglobulinas presentan muchísima diversidad. El número total de
especificidades de anticuerpos disponibles en un individuo se conoce con el
nombre de repertorio de anticuerpos o de inmunoglobulinas y en el ser humano,
ese número, es por lo menos de cien mil
millones. Antes de que se pudieran analizar directamente los genes que
codifican para las Ig, existían dos teorías que intentaban explicar el origen
de semejante diversidad. La TEORÍA DE LA LÍNEA GERMINAL postulaba que existía
un gen distinto para cada cadena de Ig diferente y, por lo tanto, proponía que
el repertorio de Ig era hereditario. Por el contrario, la TEORÍA DE LA
DIVERSIFICACION SOMÁTICA postulaba que el amplísimo repertorio se generaba a
partir de un conjunto de genes hereditarios que codifican para la porción
variable de las las Ig los cuales se modificaban de una manera particular en
cada una de las células B. El clonado de los genes de las Ig reveló que, tal
como proponía esta última teoría, la generación de diversidad se produce por
rearreglos del ADN que codifica para las porciones variables de las Ig durante el desarrollo de los linfocitos B.
Las
cadenas H y L de las Ig están codificadas por distintos grupos de genes y, para
cada una de las cadenas, existen varios fragmentos génicos involucrados en la
generación de sus porciones variables. En las células que darán lugar a los
linfocitos B, estos fragmentos génicos se rearreglan a través de un proceso que
se conoce con el nombre de recombinación
somática (Figura 4).
|
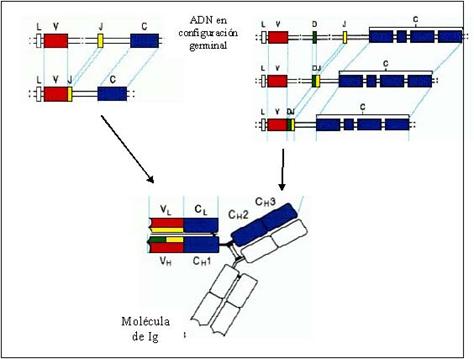
|
Figura 4: Recombinación somática. La porción variable de la cadena L (VL)
se constituye por combinación de fragmentos denominados V (rojo) y J
(amarillo), mientras que la región variable de la cadena H (VH)
involucra, además, fragmentos D (verde). Los fragmentos génicos presentes en el
ADN en configuración germinal sufren el proceso de recombinación somática,
dando lugar a una combinación única de fragmentos V-J para la porción VL
y V-D-J para la región VH en cada linfocito B.
Hasta aquí
hemos visto de qué manera es posible que se constituya la porción variable de
las cadena L y H pero, para simplificar, hemos presentado las cosas como si
sólo existiera una copia de cada uno de los genes involucrados en el proceso de
recombinación somática. En realidad, en el ADN en configuración germinal,
existen múltiples copias de cada uno de los genes involucrados en este proceso
y es la selección de un segmento u otro lo que hace posible la gran diversidad
de regiones variables entre las distintas Ig. La unión entre los fragmentos
recombinados (VL-JL ó VH-DH-JH)
es imprecisa, lo cual es una fuente extra de variabilidad para la porción
variable de las Ig. Los rearreglos del ADN que generan proteínas no funcionales
se denominan "no-productivos" y suelen ser los más frecuentes. Para
que un linfocito B pueda desarrollarse normalmente debe lograr un rearreglo
productivo de su Ig, de no ser así, no podrá continuar con su desarrollo y
morirá por apoptosis.
Etapas de maduración de los linfocitos B
Tal como
hemos mencionado anteriormente, las células B maduran mayoritariamente en la medula ósea. El desarrollo de los linfocitos B depende
de la presencia de células estromales que actúan, no sólo como una red de
sostén necesaria para que los linfocitos B continúen su desarrollo, sino
también como fuente de factores de crecimiento críticos que estimulan la
diferenciación y proliferación.
En el
primer estadio de diferenciación, conocido con el nombre de estadio pro-B, los linfocitos poseen una
capacidad limitada de auto-renovación. Durante este estadio es que se produce
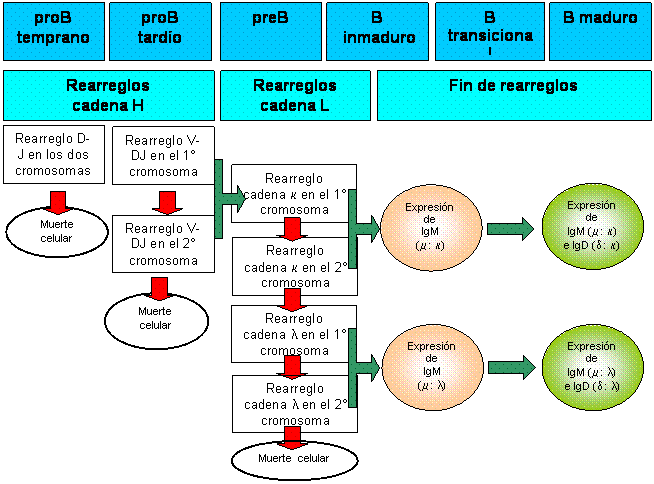
el rearreglo de la cadena H de las Ig, el cual se lleva a cabo en dos etapas:
primero se asocian los fragmentos DH-JH (pro-B temprano)
y luego se une el fragmento VH al DHJH
previamente rearreglado (pro-B tardío). Tal como se observa en la Figura 5, la asociación DH-JH
se produce en ambos cromosomas. Por el contrario, la unión del fragmento VH
al DHJH se intentará primeramente en un cromosoma y en
caso de no ser exitoso, se intentará rearreglar el segundo cromosoma. Este
fenómeno se conoce con el nombre de exclusión
alélica y garantiza que sólo se exprese la cadena H de uno de los dos
alelos del genoma.
|
|
Figura 5
La ausencia
de rearreglos exitosos de la cadena H lleva a la apoptosis del linfocito B. El
rearreglo productivo de la porción VH permite la expresión en la membrana de
una cadena pesada m (Hm) asociada con dos proteínas producidas por el
linfocito que están unidas en forma no covalente constituyendo una cadena
liviana sustituta (Ls). El ensamblado de la cadena H rearreglada a la cadena Ls
y su asociación al heterodímero IgaIgb
en la membrana del linfocito constituye el pre-BCR. La presencia del pre-BCR en
la membrana caracteriza el siguiente estadio de maduración denominado pre-B, en donde los linfocitos finalizan
con los rearreglos de la cadena H, realizan varios ciclos de proliferación y
comienzan posteriormente a rearreglar la cadena L. De esta manera, cada una de
las células hijas de la progenie que poseen genes de cadena H ya rearreglados
recombinan en forma independiente los fragmentos de la porción variable de la
cadena L, aumentando nuevamente la diversidad. Para que todo esto sea posible,
se necesita la transducción de señales de sobrevida del pre-BCR. Si bien hasta
el momento no está claro qué es lo que gatilla la transducción de la señal a
través de dicho receptor, existen evidencias que indican que la proteína
quinasa Btk está involucrada. En este sentido, los pacientes que presentan
mutaciones en dicha proteína (enfermedad de Bruton) poseen los linfocitos
arrestados en el estadio pro-B.
Los
rearreglos de la porción variable de la cadena L también están gobernados por
el fenómeno de exclusión alélica e involucran la asociación de fragmentos VL
y JL.. Existen dos tipos distintos de cadena L:, la cadena liviana
kappa (Lk)
o la lambda (Ll).
Primeramente se intentará un rearreglo productivo de la cadena Lk en uno de
lo cromosomas y, en los casos en que no se consiga, se procederá a intentar
rearreglar esa misma cadena en el otro cromosoma. Si estos intentos no fueran
exitosos, comenzarán los rearreglos de la cadena Ll, primero
en un cromosoma y luego en el otro. Normalmente, un 65% de linfocitos B logra
un rearreglo exitoso de cadena Lk,
mientras que el restante 35% presenta rearreglos productivos de la cadena Ll. No
existen linfocitos con rearreglos no productivos de cadena L ya que éstos no
son viables y mueren por apoptosis.
Una vez que
los genes de la cadena L son rearreglados exitosamente, la cadena L comienza a
sintetizarse y se combina con la cadena Hm a fin de
formar la molécula de IgM. Dicha molécula se expresará en la membrana junto con
el heterodímero Iga-Igb
constituyendo el BCR de clase IgM característico del estadio B inmaduro.
En
las etapas de maduración de los linfocitos B que hemos visto hasta el momento
lo crucial es generar rearreglos productivos de los genes de cadena H y L que
permitan la expresión de una molécula de Ig en la membrana. Aquellas células
que logran generar su receptor antigénico y expresarlo pueden avanzar a la
siguiente etapa de maduración, en donde los mecanismos de control cambian el
foco de atención hacia la especificidad del BCR. Es decir que, una vez que el
linfocito alcanza el estadio B inmaduro y expresa el BCR en la membrana , dicho
receptor será evaluado en función de su capacidad de reconocer antígenos
presentes en el ambiente del órgano linfático primario. La finalidad de esta
"evaluación" es controlar a aquellos linfocitos cuyos BCR pueden
reconocer moléculas propias, los cuales serían potencialmente peligrosos ya que
podrían generar respuestas de tipo autoinmunes. Este proceso de
"evaluación" se conoce como inducción de tolerancia central. La especificidad y la avidez del receptor por
esos antígenos determinará el camino a seguir por el linfocito: sobrevivir y
continuar madurando, o morir por apoptosis sin alcanzar la madurez.
Inducción de tolerancia central de linfocitos B
Los
linfocitos B inmaduros que no reciban señal alguna a través de su BCR en la
médula ósea, son capaces de salir del órgano para continuar con su proceso de
maduración en el bazo. Por el contrario, aquellos linfocitos B inmaduros
capaces de reconocer antígenos propios en la médula ósea son considerados
peligrosos y "controlados" a través de diversos mecanismos dependiendo
de la intensidad de la señal recibida por el BCR. Es así, que los que reciben una señal intensa a
través del BCR morirán por apoptosis en la medula ósea. Antes de morir, al
linfocito B inmaduro se le da la oportunidad de reemplazar el BCR autorreactivo
por otro que no lo sea, a fin de evitar la muerte por apoptosis. Este proceso
se conoce con el nombre de edición del
receptor. Si el nuevo BCR generado no es autorreactivo, el linfocito B
inmaduro no entra en apoptosis y sale de la médula ósea para continuar su
proceso de maduración. Si los distintos intentos de "editar" el BCR
continúan generando un receptor autorreactivo, la célula morirá por apoptosis
en la médula ósea.
Por otro
lado, aquellos linfocitos B inmaduros que en la médula ósea reciban señales
débiles a través de su BCR, serán inactivados y entrarán en un estado
permanente de no-respuesta, también denominado anergia. Estos linfocitos autorreactivos abandonan la médula ósea
pero, al no ser capaces de activarse en la periferia, mueren relativamente
pronto.
Vale la
pena mencionar que, dado que no todos los antígenos propios pueden alcanzar la
médula ósea a fin de protagonizar la inducción de tolerancia central B, muchos
de los linfocitos B que continúan con su proceso de maduración poseen BCR
capaces de interaccionar con moléculas propias. Dichos linfocitos son
controlados en la periferia, a través de mecanismos de inducción de tolerancia periférica.
Maduración periférica de linfocitos B
Del total
de linfocitos B inmaduros que se genera diariamente sólo un pequeño porcentaje
logra salir de médula ósea y alcanzar el bazo, donde continúan con su proceso
de maduración. ¿Por qué se generan tantos linfocitos B inmaduros y sólo algunos
sobreviven? Todavía esta pregunta sigue sin tener una respuesta clara pero
probablemente, la mayoría de los linfocitos B inmaduros sean seleccionados
negativamente en la médula ósea durante la inducción de tolerancia central
debido a que sus BCR son capaces de reconocer moléculas propias. Sólo aquellos
linfocitos B inmaduros, que sobrevivan a la inducción de tolerancia central,
saldrán de la médula ósea hacia el bazo, el órgano donde culminarán su
maduración. En este estadio los linfocitos B, que se encuentran en la periferia
en un estado de transición entre el estadio B inmaduro y maduro, reciben el
nombre de linfocitos B transicionales
(BTr). Dentro de esta población de
linfocitos pueden diferenciarse dos subpoblaciones bien definidas, BTr de tipo
1 (BTr1) o de tipo 2 (BTr2), que se encuentran en el bazo ubicadas en distintos
lugares anatómicos.
Durante el
estadio BTr1, los BCR de dichos linfocitos también son "controlados"
y sufren un proceso de selección negativa si reciben señales a través de su BCR
para reconocer moléculas propias. A través de este mecanismo de inducción de
tolerancia periférica, nos aseguramos que los linfocitos B autorreactivos que
han sobrevivido a la inducción de tolerancia central en la médula ósea no
continúen su desarrollo y mueran por apoptosis en el bazo. Posteriormente, aquellos
sobrevivientes, darán lugar a los BTr2, los cuales aparentemente necesitan
recibir señales de sobrevida a través de su BCR, aún no bien definidas, para
alcanzar el estadio de B maduro.
Numerosas
evidencias demostraron que es necesaria además la presencia de ciertos factores
de sobrevida, tales como la citoquina BAFF, para la transición de los
linfocitos BTr1 hacia el estadio BTr2 y B maduras. Una vez que los linfocitos
han alcanzado su madurez, co-expresan en su membrana BCR de tipo IgM e IgD, sin
embargo presentan una única especificidad dada por la porción variable de las Igs, que es idéntica. Esto se explica
gracias a que una misma porción VH generada por recombinación somática puede
asociarse con los genes Cm (para dar la IgM) ó Cd (para dar
la IgD).
Conclusiones
Los
linfocitos B, al igual que el resto de las células del sistema inmune, se
originan en la médula ósea a partir de un precursor común. Existen miles de
millones de linfocitos B distintos entre sí, cada uno de los cuales expresa en
su membrana un receptor antigénico particular. La naturaleza se las ha
ingeniado para generar semejante diversidad de receptores utilizando sólo un
conjunto de genes, los cuales son rearreglados en forma distinta en cada uno de
los linfocitos B en desarrollo.
Debido a
cómo se generan las inmunoglobulinas, una vez que el BCR puede ser expresado en
la membrana, necesariamente deben existir mecanismos de control que evalúen la
especificidad del mismo. Si bien durante la ontogenia de linfocitos B la
mayoría de las células mueren por apoptosis antes de alcanzar la madurez, este
proceso, lejos de ser un gasto innecesario de energía, mantiene el delicado
equilibrio entre la diversidad y la autoinmunidad. El proceso de generación de
las inmunoglobulinas nos asegura la gran diversidad necesaria para estar
protegidos contra la amplísima variedad de microorganismos existentes, sin
embargo esta situación acarrea conjuntamente la aparición de rearreglos capaces
de interaccionar con moléculas propias. Es por ello que existen numerosos
mecanismos de control para evaluar la especificidad de las inmunoglobulinas
generadas, a fin de evitar la aparición de fenómenos autoinmunes.
Aquellos
linfocitos que sobreviven a los mecanismos de control y alcanzan el estadio B
maduro, co-expresan en su membrana BCR de
tipo IgM e IgD, los cuales son específicos para antígenos que aún no conocen,
por lo que también reciben el nombre de linfocitos B vírgenes. Dichas células
comienzan un tráfico linfocitario en busca del antígeno para el cual son
específicas y, aquellas que lo encuentren, podrán activarse, proliferar y
diferenciarse a células productoras de anticuerpos. Estos anticuerpos tendrán
la capacidad de reconocer al antígeno específico y reclutar distintos
mecanismos efectores a fin de destruirlo.
Agradecimientos:
A la Dra. Mirta Giordano, por su
crítica revisión del manuscrito.
Referencias.
Tonegawa
S., 1983. Somatic generation of antibody diversity.
Nature,
302:575.
D
Zipori , 1992. The renewal and differentiation of hemopoietic
stem cells.
FASEB
J., 6:2691.
Gay
D, Saunders T, Camper S,Weigert M., 1993. Receptor editing: an approach by
autoreactive B cells to escape tolerance. Journal Experimental Medicine,
177:999.
Mc
Sandel
PC, Monroe JG., 1999. Negative selection of
immature B cells by receptor editing or deletion is determined by site of
antigen encounter. Immunity, 10:289.
Marcel
Batten,Joanna Groom,Teresa G. Cachero, Fang Qian, Pascal Schneider,Jurg
Tschopp,Jeffrey L. Browning,Fabienne Mackay, 2000. BAFF Mediates Survival of
Peripheral Immature B Lymphocytes. Journal Experimental Medicine,
192:1453.
Richard
R. Hardy, yoko Hayakawa, 2001. B cell development pathways.
Annual
Review of Immunology, 19:595.
Charles
Janeway, Paul Travers, Mark Walport, Mark Shlomchik, 2001. Immuno Biology. The
immune system in health and disease. 5th edition,
Stephen
B. Gauld, Joseph M. Dal Porto, John C. Cambier, 2002. B Cell Antigen Receptor
Signaling: Roles in Cell Development and Disease. Science, 296:1641.
Freddy
Radtke, Anne Wilson and H Robson MacDonald, 2004. Notch signaling in T- and
B-cell development. Current Opinion in Immunology, 16:174.
Antonius
G. Rolink, Jan Andersson, Fritz Melchers, 2004. Molecular mechanisms guiding
late stages of B-cell development. Immunological Reviews, 197:41.
Thomas
T. Su, Beichu Guo, Bo Wei, Jonathan Braun, David J. Rawlings, 2004. Signaling
in transitional type 2 B cells is critical for peripheral B-cell development.
Immunological
Reviews, 197:161.
Mila
Jankovic, Rafael Casellas, Nikos Yannoutsos, Hedda Wardemann, Michel C.
Nussenzweig, 2004. Rags and regulation of autoantibodies. Annual Review of
Immunology, 22:485.
*
Dra. Romina Gamberale.
Laboratorio de Inmunología,
IIHema, Academia Nacional de Medicina.
E-mail:
rgamberale@hematologia.anm.edu.ar
|
|
Revista QuímicaViva Número 3, año 3, septiembre 2004 quimicaviva@qb.fcen.uba.ar |