¿Qué relación hay entre las enfermedades virales y el lugar dónde ocurren?
María Laura Morell
Laboratorios de Estrategias Antivirales y Procesos Moleculares de la Interacción Virus-Célula, Departamento de Química Biológica, Facultad de Ciencias Exactas y Naturales, Universidad de Buenos Aires.
Recibido: 10/04/2024 - Aceptado: 20/04/2024
Resumen
Los virus son microorganismos formados por biomoléculas: ácidos nucleicos, proteínas, lípidos e hidratos de carbono. Su genoma puede ser de ADN o ARN. Dichos microorganismos infectan a diversos organismos ya sean vectores u hospedadores. Los virus ingresan al organismo y lo infectan. Si replican y no lo afectan, sólo transmiten el virus, se trata de vectores; por el contrario, cuando el virus replica y el organismo se ve afectado, se trata de un hospedador. Existen diversos tipos de vectores que habitan en distintas regiones del mundo y transmiten diferentes virus. Algunos de esos vectores son mosquitos, ganado, aves, roedores o personas, entre otros. La forma de transmisión del virus depende del tipo de vector y del tipo de virus. Las enfermedades que producen los virus, como en el caso de las fiebres hemorrágicas pueden resultar mortales si no son tratadas a tiempo. Es por este motivo que es esencial conocer cuáles son sus vectores, hospedadores, hábitats y cómo prevenir el contagio.
Palabras clave: virus, vector, huésped, hábitat, enfermedad
Summary
Viruses are microorganisms composed by molecules: nucleic acids, proteins, lipids and carbohydrates. Their genomes can be DNA or RNA. Such microorganisms infect a variety of organisms, vectors or hosts. Viruses enter the organism and infect it. If they replicate and do not affect it, they only transmit the virus, that organism is a vector; on the contrary, when the virus replicates and affects the organism, the organism is a host. There are diverse types of vectors that live in distinct regions of the world and transmit different viruses. Some of these vectors are mosquitoes, cattle, birds, mice or persons, among others. Virus transmission depends on the type of vector and virus, respectively. Diseases caused by viruses could be mortal if not treated. This is the main reason why it is essential to know which their vectors, hosts, habitats are and how to prevent contagion.
Keywords: virus, vector, host, habitat, disease
La palabra virus ha sido ampliamente escuchada, leída, escrita, hablada, temida, diagnosticada y sufrida por casi toda la humanidad durante la pandemia provocada por el severe acute respiratory syndrome coronavirus 2 (SARS-CoV-2) causante de la enfermedad coronavirus disease 2019 (COVID-19) [1].
El término virus, tiene su origen en el latín virus que significa toxina o veneno. El nombre, surgió a partir de que unos científicos realizaron ensayos con extractos de plantas de tabaco afectadas por la enfermedad del mosaico y los filtraron, comprobando que en dichos filtrados continuaba presente la toxina o veneno que producía la enfermedad [2].
Los virus son microorganismos formados por biomoléculas, es decir, son una asociación de ácidos nucleicos, proteínas, hidratos de carbono y lípidos. Su genoma puede estar constituido por ácido desoxirribonucleico (ADN) o por ácido ribonucleico (ARN) (Figura 1). Los virus con genoma a ADN tienden a ser más estables que los virus con genoma a ARN pues el ADN está formado por 2 hebras que se aparean y mantienen unidas mediante puentes de hidrógeno, mientras que el ARN suele ser monocatenario y más susceptible a la acción de las enzimas que lo degradan. Por otro lado, los virus a ARN tienen una tasa de mutación más alta que la de los virus a ADN ya que la ARN polimerasa carece de actividad "correctora" al polimerizar los nucleótidos.
Dicho genoma puede estar asociado o no a proteínas denominadas nucleoproteínas. La/s molécula/s de ácido nucleico (en plural ya que puede estar segmentado) están delimitadas por un conjunto de proteínas que forman la cápside del virus. A lo largo de esta cápside, se encuentran inmersas las glicoproteínas, es decir, proteínas asociadas a glúcidos, o sea, hidratos de carbono (Figura 1). Estas moléculas son la estructura del virus que interactúa con los receptores celulares y posibilita la entrada a la célula y por ende su infección [3].
Si la estructura del virión culmina con la cápside entonces se habla de un virus desnudo. Si la cápside está envuelta por una bicapa de lípidos entonces se trata de virus envueltos. Esto marca una gran diferencia ya que, por lo general, los virus envueltos son menos resistentes que los desnudos. Esta diferencia se debe a que los virus envueltos son más lábiles a los cambios de temperatura, de pH y efecto de desengrasantes (jabones, detergentes) y desinfectantes (etanol, lavandina) [4]. ¿Recuerdan el uso continuo de etanol 70° durante la pandemia de 2020?
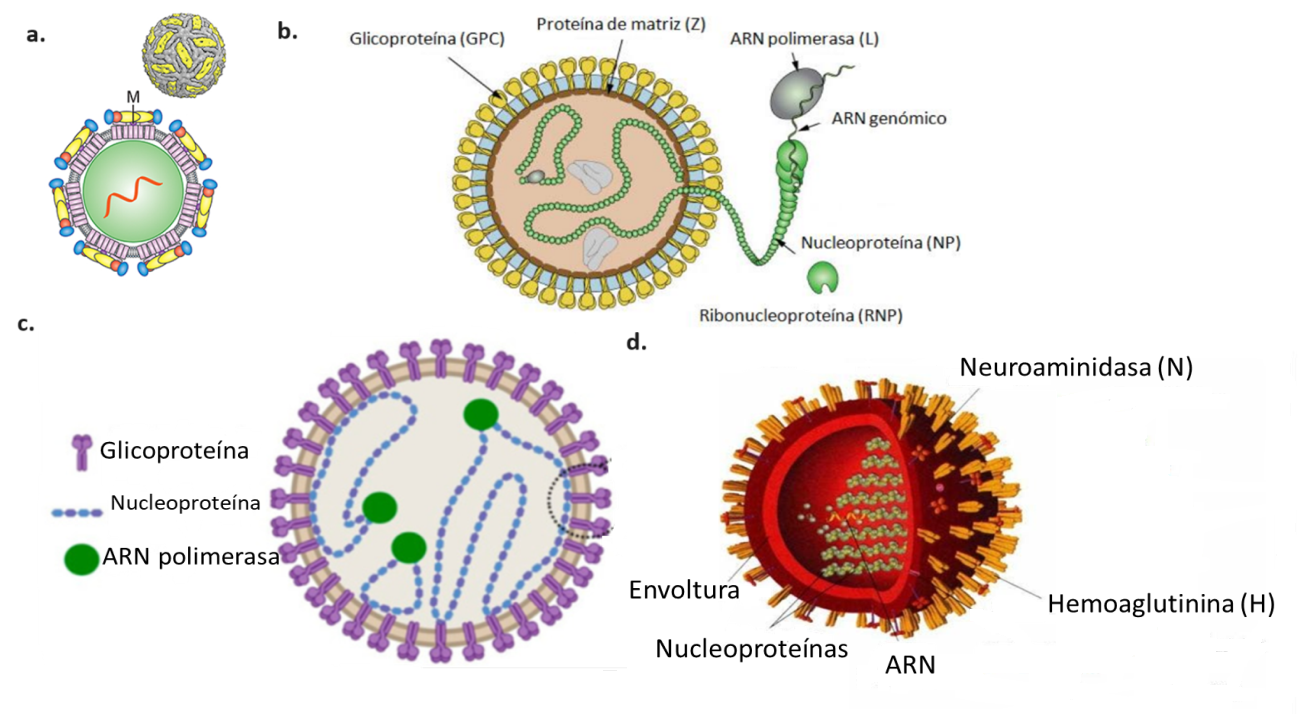
Figura 1: Estructura de los viriones de a. flavivirus, b. arenavirus, c. hantavirus, d. influenza. Se indican los ácidos nucleicos, nucleoproteínas, polimerasa viral, envoltura y glicoproteínas. Imágenes adaptadas de Pierson y Diamond, 2020; Instituto de Bioinformática Suizo [SIB], 2021; Meier et al., 2021; Futura Sciences, 2024.
A diferencia de las bacterias que son organismos unicelulares, los virus, son parásitos intracelulares obligados. Esto implica que los virus no replican por sí mismos sino que requieren de un vector u hospedador que les provea un ambiente adecuado para su replicación. Surge entonces un interrogante: ¿Es lo mismo un vector que un hospedador? ¿Cuál es la relación entre los virus, sus vectores y sus hospedadores? Vamos por partes. Un vector es un organismo en el cual el virus puede replicar y amplificarse, es decir, generar más copias de sí mismo porque existe una adaptación entre virus y vector que posibilita la convivencia. Esto hace que el virus pueda replicar sin generar efectos dañinos sobre el vector, en otras palabras, que no lo enferme. Por otro lado, los hospedadores son organismos infectados por los virus. Estos últimos replican y generan copias de sí mismos ocasionando consecuencias en dicho organismo, es decir, lo afecta o enferma. Hay virus que son transmitidos por vectores a las personas, esto convierte a los vectores en “intermediarios” entre el virus y el hospedador [5] (Figura 2).
Figura 2: Relación entre virus- vector y hospedador.
Esto abre nuevos interrogantes: ¿Cuáles son los vectores y/o hospedadores de los virus? ¿Dónde se encuentran?
Virus transmitidos por mosquitos
El mayor vector viral a nivel mundial es... el mosquito. Los mosquitos son vectores de numerosas especies de virus, entre ellos, virus de la familia Flaviviridae: virus del dengue, Zika, chikungunya, fiebre amarilla y West Nile. Los mosquitos habitan en regiones húmedas con climas cálidos, encontrando un nicho ideal en los ambientes tropicales. Estas condiciones pueden encontrarse en América en la región cercana al trópico de Ecuador, centro de África, sudeste asiático y norte de Australia [6]. Últimamente, debido al cambio climático, los climas templados de distintas regiones de Argentina se han tropicalizado. Los veranos se tornaron más cálidos y húmedos, con tormentas intensas que provocan gran caída de agua en poco tiempo lo que deriva en anegamiento, lagunas, charcos y demás cuerpos de agua estancada. Esto favorece la proliferación del mosquito [7]. Al aumentar el número de individuos de la población, aumenta también la probabilidad de que esos mosquitos sean portadores de algunos de los flavivirus antes mencionados. Esto implica que el área de incidencia de las enfermedades causadas por los mosquitos se ha expandido desde sus regiones originales (Figura 3).
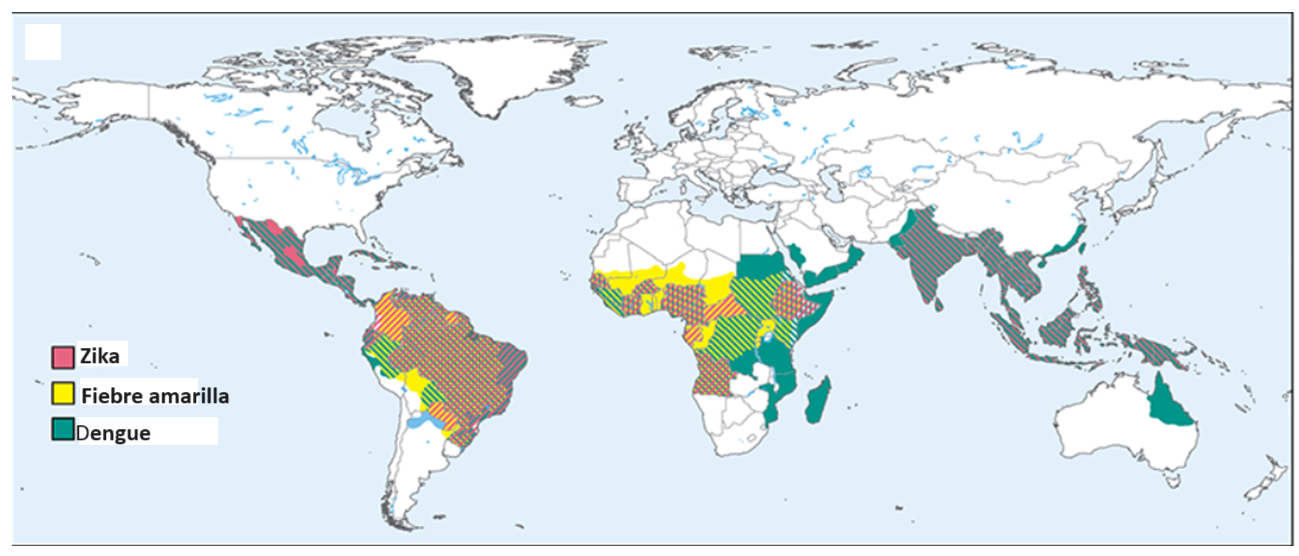
Figura 3: Área de incidencia de las enfermedades Zika, fiebre amarilla y dengue a nivel mundial. Adaptado de Pierson y Diamond, 2020.
Las enfermedades llevan el mismo nombre de los virus que le dan origen y todas se caracterizan por generar como síntomas: fiebre elevada, fibromialgia, cefalea y dolor en las articulaciones. La transmisión es a través del mosquito, no existe transmisión horizontal de persona a persona. La excepción es la del virus Zika, existen estudios que demuestran que el virus puede atravesar la placenta y la madre infectada, infectar al bebé, que al nacer puede presentar microcefalia. También se ha demostrado que el virus Zika se transmite por vía sexual a través del semen [6]. La transmisión del virus ocurre cuando el mosquito pica a una persona infectada con alguno de estos flavivirus. La hembra del mosquito es quien pica pues su probóscide es lo suficientemente fuerte para atravesar la epidermis y acceder a la sangre. Al picar, inyecta su saliva con anticoagulantes que vuelven a la sangre más líquida para poder succionarla. Al succionar la sangre de una persona infectada con algún flavivirus, el virus pasa de la sangre de la persona al mosquito. Los mosquitos hembra requieren de la sangre humana porque obtienen el factor de crecimiento necesario para la ovoposición.
Aedes aegypti y Aedes albopictus son los vectores de los virus del dengue, Zika, chikungunya y fiebre amarilla (Figura 4) [8, 9] mientras que los mosquitos del género Culex transmiten el virus de West Nile [10].

Figura 4: Mosquitos Aedes aegypti (izquierda) y Aedes albopictus (centro), vectores de los virus Zika, dengue, chikungunya y fiebre amarilla. Se caracterizan por presentar anillos blancos en sus patas. Mosquitos del género Culex, transmisores del virus West Nile (derecha). Imagen izquierda: Muhammad Mahdi Karim, 2019; Centro: James Gathany, CDC ID#2165; Derecha: CDC, Division of vector-borne diseases 2022.
Virus transmitidos por ganado/aves -personas
Otro ejemplo cotidiano lo constituye el virus influenza, agente etiológico de la gripe. Los hospedadores son los animales: ganado porcino, aves de corral y humanos. El virus pertenece a la familia Orthomyxoviridae. Los miembros de esta familia, presentan el genoma segmentado en 6, 7 u 8 fragmentos de diferente tamaño (Figura 1d). Los genes codifican para distintas proteínas, entre ellas, 2 glicoproteínas: la hemaglutinina (H) y la neuraminidasa (N). Dichas glicoproteínas son reconocidas por receptores de los hospedadores, por lo cual, resultan clave en el proceso de infección [11]. La mayoría de los virus con genoma de ARN, al replicar, producen errores en su copiado por acción de la ARN polimerasa viral generando mutaciones puntuales. La acumulación de mutaciones puntuales a lo largo del tiempo conduce al antigenic drift o cambio antigénico que genera un cambio en las glicoproteínas virales H y N. Este tipo de cambio, provoca que circulen nuevas cepas de influenza todos los años y por ende, que sea necesario desarrollar nuevas vacunas anualmente. Por otro lado, al tratarse de virus con genoma segmentado puede ocurrir, con menos frecuencia, que 2 cepas distintas infecten al mismo organismo. Por ejemplo, influenza aviar e influenza porcina que infecten al mismo cerdo. En ese caso, puede ocurrir un reordenamiento de los fragmentos de genoma en el hospedador y producirse una nueva cepa que infecte a otro hospedador. Este cambio abrupto se denomina antigenic shift y es el que genera el “salto de especie”, es decir, genera un cambio tan radical en la estructura del virus que genera un nuevo tipo de virus que pude infectar a otros organismos [12]. Esto sucedió cuando el virus de la gripe aviar influenza A subtipo H5N1, mutó y empezó a infectar a los humanos o cuando se produjo la pandemia de gripe porcina por el virus Influenza A subtipo H1N1 que también mutó y comenzó a infectar humanos. Las especies que infectan a los humanos son influenza A H1N1, H5N1 y H3N2 [13]. La transmisión del virus es horizontal, es decir, de animal a animal o persona a persona a través de aerosoles que se generan al estornudar, toser o hablar (las microgotas de saliva), por contacto con mucosas o secreciones con virus. Esta enfermedad es de ocurrencia mundial ya que sus hospedadores (personas, ganado y aves de corral) tienen distribución mundial. En el caso del salto de barrera de especie o antigenic shift, cada vez es más frecuente debido a las actividades de ganadería y cría de pollos y cerdos. Si el ganado se enferma, al estar los humanos en contacto con ellos, la exposición es mayor y la probabilidad de que el virus mute y comience a infectarlos también es mayor. Existen vacunas contra el virus influenza y se deben aplicar nuevamente cada año [11].
Virus transmitidos por roedores
Por otro lado, se encuentran las fiebres hemorrágicas producidas por virus de distintas familias. Así como el flavivirus dengue puede generar fiebre hemorrágica, existe otro virus que ocasiona fiebre hemorrágica en la Argentina, el arenavirus Junín. Esta enfermedad también se conoce como “mal de los rastrojos” debido a que su hospedador natural, el ratón colilargo Calomys musculinus (Figura 5), se alimenta de los restos de las cosechas de plantaciones. El nicho ecológico de este roedor es el área agrícola-ganadera de Argentina que incluye a las provincias de Buenos Aires (norte), sur de Santa Fe y sur de Córdoba.

Figura 5: Vector del arenavirus Junín causante de la fiebre hemorrágica Argentina, el ratón colilargo, Calomys musculinus. Foto: Hans Hillewaert.
La transmisión del virus del roedor al humano se da de manera directa a través del contacto de heridas en la piel con las heces o excretas de un ratón infectado o por mordedura del animal infectado. Asimismo, existe transmisión por aerosoles. Esto ocurre cuando los roedores infectados en búsqueda de comida, acceden a galpones o sitios de almacenaje de cosecha/granos y orinan y defecan. Estos residuos, se deshidratan y se convierten en polvo. Al realizar traslados de materiales o barrer, las partículas de polvo de los restos que contienen virus quedan suspendidas en el aire y la persona inhala esas partículas. Si bien existen sospechas de transmisión persona- persona, no han sido reportadas oficialmente. La infección por virus Junín genera síntomas como cualquier enfermedad infecciosa tales como fiebre, cefalea, mialgia, debilidad y malestar general. Si se trata de una cepa del virus altamente patogénica y la persona no es tratada, la infección progresa y genera una infección multisistémica, afectando al hígado, bazo y cerebro. La infección del sistema nervioso ocasiona síntomas neurológicos como olvidos espontáneos y desorientación. En su forma más grave, el virus puede replicar en las células del endotelio de los vasos sanguíneos y producir la fiebre hemorrágica. Existe una vacuna contra el virus Junín, #Candid1, la cual se produce en el Instituto Maiztegui, en Pergamino, localidad de la provincia de Buenos Aires, Argentina. Dicha vacuna es obligatoria y está incorporada al calendario argentino de vacunas a partir de los 15 años en la región endémica. El tratamiento de la enfermedad para personas infectadas no vacunadas, consiste en la administración de suero con anticuerpos neutralizantes provenientes de pacientes convalecientes o administración del fármaco antiviral ribavirina [14].
Adicionalmente, en Argentina, existe otra enfermedad ocasionada por un virus transmitido por un roedor. Se trata del hantavirus perteneciente a la familia Bunyaviridae. Dicho virus produce dos formas graves de la enfermedad: el síndrome cardiopulmonar o la fiebre hemorrágica con insuficiencia renal. En Argentina, las cepas de hantavirus que circulan, Andes y Laguna Negra, ocasionan el síndrome cardiopulmonar [15]. Los hospedadores naturales, son los roedores del género Oligoryzomys. Estos ratones, habitan en el suroeste de Argentina, cercano a la cordillera de los Andes y se alimentan de caña colihue. La floración masiva de las cañas, cada 30 años aproximadamente, provoca la “ratada”, es decir, el crecimiento exponencial de la población de roedores. Dado que disponen de recursos alimenticios abundantes, cuentan con energía suficiente para crecer y reproducirse y aumentar su tamaño poblacional a pesar de la acción de sus predadores, los búhos y lechuzas. Al aumentar el número de ratones, aumenta la probabilidad de que algún animal porte virus hanta. El hantavirus se transmite de igual manera que el virus Junín, por aerosoles o por entrar en contacto con excretas u orina del animal infectado y ocasiona los mismos síntomas. En 2018, hubo un brote de hanta en la localidad de Epuyén, Chubut, Argentina. Dicho brote se debió a la concurrencia a una fiesta de una persona infectada con la cepa Andes de hantavirus. Contagió al resto de los asistentes y ese fue el primer caso de transmisión horizontal a nivel mundial de hantavirus [16]. No existe vacuna contra el virus hanta y el tratamiento para las personas infectadas consiste en el tratamiento clínico de los síntomas.
En resumen, existen numerosos virus que pueden ser transmitidos por diversos vectores animales. Es fundamental entonces conocer qué animales transmiten virus y tomar acciones preventivas ya sea combatiéndolos, evitando el contacto con ellos y/o extremando las medidas de precaución al interactuar con los hábitats naturales de dichos vectores.
Moraleja de esta historia viral: si van a viajar, investiguen qué enfermedades endémicas hay y si existen vacunas contra los patógenos causantes de dichas enfermedades.
Referencias:
1. Jackson CB, Farzan M, Chen B, Choe H (2022) Mechanisms of SARS-CoV-2 entry into cells. Nat Rev Mol Cell Biol Jan, 23(1):3-20. doi: 10.1038/s41580-021-00418-x. Epub 2021 Oct 5 PMID: 34611326
2. Mammas IN, Drysdale SB, Theodoridou M, Greenough A, Spandidos DA (2020) Viruses, vaccinations and RSV: Exploring terminology in paediatric virology. Exp Ther Med. Dec, 20(6):300. doi: 10.3892/etm.2020.9430.
3. Madjoul S, Compton AA (2022) Lessons in self-defence: inhibition of virus entry by intrinsic immunity. Nat Rev Immunol Jun,22(6):339-352. Doi: 10.1038/s41577-021-00626-8. Epub 2021 Oct 13. PMID: 34646033
4. Brackley CA, Lips A, Morozov A, Poon WCK, Marenduzzo D (2021) Mechanisms for destabilisation for RNA viruses at air-water and liquid-liquid interfaces. Nat Commun Nov 24,12(1):6812. Doi: 10.1038/s41467-021-27052-7. PMID: 34819516
5. Schneider CA, Calvo E, Peterson KE (2021) Arboviruses: How saliva impacts the journey from vector to host. Int J Mol Sci Aug25,22(17):9173. doi: 10.3390/ijms22179173. PMID: 34502092
6. Pierson TC, Diamond MS (2020) The continued threat of emerging flaviviruses. Nat Microbiol Jun,5(6):796-812. Doi: 10.1038/s41564-020-0714-0. Epub 2020 May 4. PMID: 32367055
7. López MS, Gómez AA, Müller GV, Walker E, Robert MA, Estallo EL (2023) Relationship between climate variables and dengue incidence in Argentina. Environ Health Perspect. May,131(5):57008. doi: 10.1289/EHP11616. Epub 2023 May 24. PMID: 37224070
8. Nazareth T, Seixas G, Lourenco J, Bettencourt PJG (2023) Aedes albopictus arrives in Lisbon: an emerging public health threat. Front Public Health Dec 19,11:1332334. Doi: 10.3389/fpubh.1332334 PMID: 38169710
9. Souza_Neto JA, Powell JR, Bonizzoni M (2019) Aedes aegypti vector competence studies: A review. Infect Genet Evol Jan,67:191.209. doi: 10.1016/j.meegid.2018.11.009 Epub 2018 Nov 19 PMID: 30465912
10. Martinet JP, Bohers C, Vazeille M, Ferté H, Mousson L, Mathieu B et al. (2023) Assessing vector competence of mosquitoes from northeastern France to West Nile virus and Usutu virus. PLoS Negl Trop Dis Jun 5,17(6):e0011144. Doi: 10.371/journal.pntd.00111444 PMID: 37276229
11. Treanor JJ (2020). Influenza viruses, including avian influenza and swine influenza. En: Bennett, J.E., Dolin, R., Blaser, M.J., eds. Mandell, Douglas and Bennett’s Principles and Practice of Infectious Diseases. 9th ed. Philadelphia, PA: Elsevier, Capítulo 165.
12. https://www.encyclopedie-environnement.org/en/zoom/genomic-reassortments-a-major-source-of-influenza-pandemics/ , accesado 19/04/2024
13. https://espanol.cdc.gov/flu/about/keyfacts.htm , accesado 12/04/2024
14. Radoshitzky SR, de la Torre JC (2020) Human Pathogenic Arenaviruses. Reference module in Life Sciences. doi: 10.1016/B978-0-12-814515-9.00014-X
15. Meier K, Thorkelsson SR, Quemin ERJ, Rosenthal M (2021) Hantavirus replication cycle- an updated structural virology perspective. Viruses Aug 6,13(8):156. Doi: 10.3390/v13081561 PMID: 34452426
16. http://sobrelatierra.agro.uba.ar/estudian-en-detalle-la-transmision-del-hantavirus-en-la-patagonia/, accesado 11/04/2024
|
Revista QuímicaViva Número 1, año 23, Abril 2024 quimicaviva@qb.fcen.uba.ar |