Bacteriófagos: su importancia en los inicios de la biología molecular
Carmen Sanchez de Rivas
Departamento de Química Biológica. Facultad de Ciencias Exactas y Naturales. Universidad de Buenos Aires. IQUIBICEN. CONICET. Buenos Aires. Argentina
Resumen
En este trabajo se analizan los antecedentes, las motivaciones de los investigadores y las relaciones entre los diferentes laboratorios que permitieron el nacimiento de la biología molecular. Fue durante un periodo de 25 años (1940-1965) que se realizaron los principales trabajos científicos que tuvieron esencialmente a los bacteriófagos (fagos o virus de bacterias) y a sus hospedadores, las bacterias, como principales protagonistas. En la actualidad los fagos siguen siendo un material interesante ya sea en investigaciones básicas como evolución o en aplicaciones como ser la fagoterapia, una alternativa al uso de antibióticos.
Palabras clave: fagos, biología molecular
Summary
In this work the different approaches, researchers and laboratories involved in the emergence of a new discipline: the Molecular Biology are analyzed. Twenty-five years, from 1940 to 1965, have been enough to bring the essential papers that settled the new discipline. Bacteriophages (phages or bacterial viruses) and their bacterial hosts were essentially the vedettes of such studies. Phages also continue to support new interesting insights in basic studies as evolution or in biotechnological applications like phage therapies, an alternative to the antibiotics use
Keywords: phages, Molecular Biology
Breve resumen histórico sobre el advenimiento de la biología molecular
Fue en la segunda mitad del siglo XIX que la microbiología como ciencia se impuso y sentó sus bases esencialmente gracias a los trabajos de Louis Pasteur, Robert Koch, Josef Lister y Elias Metschnikoff poniendo fin a la teoría de la generación espontánea de los gérmenes y favoreciendo el aislamiento y estudio de cultivos puros.
Los nuevos hallazgos tuvieron aplicaciones en medicina: métodos de aislamiento y clonado, cultivos puros, relación micro-organismos con patogénesis, producción de vacunas y en procesos industriales: fermentación alcohólica.
La microscopía y los análisis químicos habían permitido caracterizar las distintas estructuras (envolturas, mitocondrias, núcleos, apéndices) que componían las células y su composición química (polisacáridos, ácidos nucleicos, proteínas). Pero se desconocía cómo los componentes interactuaban y participaban en la transmisión genética. La célula era un “todo” con sus propiedades “buenas” o “malas”, pero no se había puesto en evidencia ninguna estructura en particular responsable de transmitir los caracteres hereditarios ni sus mecanismos.
¿Cómo explicar vida y herencia?
A partir de fines de los años 30 del siglo XX, varios investigadores provenientes de diferentes disciplinas científicas formularon estas y otras preguntas destinadas a responder y caracterizar los elementos y mecanismos responsables de la transmisión de los caracteres hereditarios. Es importante señalar el invaluable aporte de los físicos. En la década del 30 en Copenhague el grupo de físicos liderado por Niels Bohr se centraron en tratar de explicar biología y herencia. Esas discusiones condujeron a Erwin Shrödinger, otro físico del grupo, a exponer algunas discusiones e interrogantes en su libro What is Life (1944). Max Delbrück, también físico, estaba presente en esos debates y las inquietudes planteadas lo condujeron a interesarse por la biología y por las formas más sencillas: bacterias y fagos como elementos de estudio. Cabe recordar que fue a principio del siglo XX que estos virus de bacterias, los bacteriófagos (o fagos) como los nombró D´Herelle, fueron descubiertos por Twort (1915) y D´Herelle (1917) [1-2-3] aunque fue este último que les dio mayor desarrollo.

Figura 1: Niels Bohr, Max Born y Max Delbrück. Copenhague,1934.
Para poder responder a esta pregunata , se requirió la asociación de:físicos como Max Delbruck, Francis Crick, Jean Weigle, Gunther Stent, Maurice Wilkins, Leo Szilard, Aaron Novick y Georges Gamov. Químicos como Linus Pauling, Frederick Sanger,y Rollin Hotchkiss.Físico-químicos como Max Perutz, y Edwin Chargaff. Médicos como Salvador Luria, François Jacob , André Lwoff y Joshua Lederberg. Biólogos como Jacques Monod, Sydney Brenner, Barbara McClintock, Alfred Hershey, Martha Chase y algunos ingenieros y matemáticos, para elaborar el conjunto de experimentos que permitieron sentar las bases de la biología molecular.
Durante ese periodo “una fiebre” particular circuló entre los investigadores provenientes de laboratorios de Inglaterra; de Estados Unidos y de Francia
Como dirá John Cairns sobre esa época en “Phages and the Origin of Molecular Biology” [3]: “fue en esos días en que nació la biología molecular y parecía que ésta sería inocente e incorruptible.” Entre el Instituto Pasteur y los otros laboratorios hubo un flujo constante de investigadores, discusiones e intercambio de material. Salvador Luria iba a Pasteur con mucha frecuencia, con cepas y fagos bajo el brazo para ensayar por ejemplo transducciones del fago P1 entre Salmonella y Escherichia coli. Eso no impidió que alguno que otro investigador retaceara tanto mutantes como fagos a sus colegas. Se cuenta que un tal A que al no obtener “directamente” un fago de B le envió una carta y utilizó el papel de la respuesta para “procesarlo” y obtener así el fago aislado!
Recordemos que muchos de los experimentos de esa época fueron realizados con el fago Lambda (λ) aislado por Ethel Lederberg [4] a principio de los años 50 a partir de un lisado deEscherichia coli tratado por UV.

Figura 2: El equipo del Institut Pasteur A.Lwoff, F. Jacob, E. Wollman y J. Monod repicando fagos para Max Delbruck. Paris,1955.
A partir de 1945 en Cold Spring Harbor, M.Delbrück, S Luria y A Herschey iniciaron el renombrado curso de verano sobre fagos .Ahí y en los simposios paralelos de biología molecular se discutían los últimos resultados, avances y propuestas de la reciente disciplina. El curso original duró hasta los años 70, y los simposios tuvieron lugar hasta 1966. Fue en uno de ellos (1953) que James Watson expuso el primer modelo de la doble hélice del DNA
En Francia, en la “Abbaye de Royaumont” cerca de París en 1952 también se realizó el Primer simposio sobre Bacteriófagos donde se reunieron la mayoría de los científicos involucrados en esa aventura

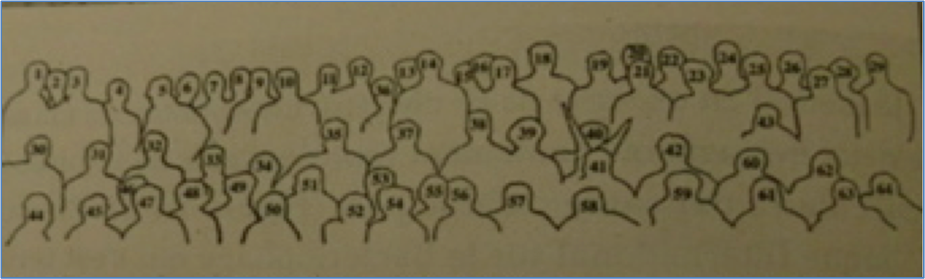
| 1.W WEIDEL | 17. R.LATARGET | 33. B. PARDEE | 49.COHEN-BAZIRE |
| 2. O. MAALOE | 18. JACOB | 34. J. SMITH | 50. B. de ROTSCHILD |
| 3. BRESCH | 19. ZSYBALSKI | 35. J. MONOD | 51. E. KELLENBERGER |
| 4.BOWDEN | 20.STENT | 36. E. WOLLMAN | 52. D. BENZER |
| 5. R. WHAL | 21.BEUMER | 37. S.BENZER | 53.M. TORRIANI |
| 6. LINDERSTOM-LANG | 22.J. BEUMER | 38. SIMINOVITCH | 54. KELLENBERGER |
| 7. P. FREDERICK | 23.M.FREDERICK | 39. DELBRÜCK | 55.H. INOSECO |
| 8. | 24.V.BONIFAS | 40. N. VISCONTI | 56. HERSCHEY |
| 9. E. EVANS | 25.M. ADAMS | 41. J.J. WEIGLE | 57. J. BERTANI |
| 10. MURRAY | 26.N.K. JERNE | 42. LEVINTHAL | 58. LEVINTHAL |
| 11. DELBRÜCK | 27. | 43. | 59. J. WATSON |
| 12. R. STANIER | 28. | 44. H.TAYLOR-EPHRUSSI | 60. RAVIN |
| 13. H. MARCOVICH | 29.A. HERSCHEY | 45. S. RAPKINE | 61. S. SPIEGELMAN |
| 14. B, EPHRUSSI | 30.P. NICOLLE | 46. LWOFF | 62. P. SLONIMSKI |
| 15. | 31.L. GORINI | 47. E.MEYNELL | 63. T. ANDERSON |
| 16.CAVALLI-SFORZA | 32.L. SILVESTRI | 48. I. STENT | 64. LWOFF |
Figura 3: Reunión de Royaumont sobre fagos, varios de los presentes recibieron el Premio Nobel.1952.
En un periodo de 25 años (1940-1965) fueron las bacterias y sus fagos los protagonistas esenciales con las cuales se realizaron los estudios que condujeron al salto cualitativo de conocimientos que dieron nacimiento a la biología molecular. Jacques Monod diría más tarde, parafraseando al “Burgués gentilhombre” de Molière: “hacíamos biología molecular sin saberlo”. Estos avances fueron posibles gracias al uso de las nuevas técnicas de microscopía electrónica, de centrifugación analítica, gradientes de sedimentación, análisis genéticos y estadísticos, análisis químicos de proteínas y ácidos nucleicos, de análisis por difracción de Rayos X y al uso de bacterias y bacteriófagos como material de estudio.
En 1957 Francis Crick propuso el término “dogma central de la Biología Molecular” para dar un marco a la hipótesis de trabajo: la información parte del DNA, y gracias al RNA mensajero (mRNA) como intermediario, permite que el código de 3 letras del DNA se convierta en un código de amino-ácidos leído por los ribosomas encargados de sintetizar las proteínas, últimos responsables en mantener la actividad celular. El término “dogma” fue criticado por algunos, entre otros por J. Monod, pues colocaría a la ciencia en una posición religiosa y ante todo incuestionable, lo contrario de lo que se espera de ella, por ser un proceso en constante construcción
A pesar de ello, el término se utilizó como marco de referencia y de trabajo, lo que permitió importantes avances pero también censuró muchos otros. Dos ejemplos lo muestran:fue difícil aceptar la existencia de controles post-transcripcionales de la expresión genética, especialmente en el Instituto Pasteur y en particular en el operón lactosa. Los estudios sobre la represión catabólica en mutantes de genes de control del operón lactosa condujeron a postular un control post-transcripcional [5]. Sólo varios años después y con nuevas evidencias se logró darle visibilidad oficial a la hipótesis [6] .También en ese mismo laboratorio, los trabajos de Mirko Beljanski sobre el rol de la transcriptasa reversa donde la información de un RNA sirve de mensajero y de molde para sintetizar DNA no fue totalmente aceptada ni valorada [7]. Sería el trabajo de Temin sobre virus con genoma de RNA, que serviría como la referencia reconocida, lo que le valdría el Premio Nobel en 1975 [8]. Por otro lado las evidencias actuales concuerdan que la vida empezó por RNAs [9] lo que demuestra cuán necesario es poner en cuestionamiento los “modelos” preexistentes para el avance de la ciencia
La similitud y transferencia de los modelos hacia organismos superiores eucariotas parecía evidente, pero aun requería comprender y explicar entre otros los procesos de diferenciación. Una humorada de Jacques Monod expresaría así esa visión: “Lo que es cierto para las bacterias Escherichia coli es cierto para los elefantes”.
Ese salto cualitativo tan importante hizo que a finales de los 60, muchos investigadores, entre ellos los del Instituto Pasteur de Paris, decidieron que “ya” se habían develado los secretos más importantes de la biología, gracias a las bacterias y sus fagos, y los abandonaron por el estudio de sistemas más complejos con la vista puesta en caracterizar procesos de embriogénesis y cáncer.
François Jacob, médico de origen, inicio un grupo de estudio de embriogénesis y carcinomas en ratas. Para un físico como Max Delbrück, todo lo que develaron los estudios sobre los mecanismos de la herencia en fagos y bacterias, no necesitaron apelar a ninguna nueva ley de la física. Su interés se centró entonces en estudiar procesos más complejos como los de diferenciación e inició un grupo de estudios en un modelo de hongos unicelulares (Phycomyces). Quizás para un físico como él, si hubiese sabido que los fagos y virus presentan la mayor diversidad de secuencias proteicas contrariamente a las encontradas entre cualquier organismo vivo desde el elefante, los humanos, la rata y las bacterias, le hubiese seducido continuar y emprender una nueva odisea.
Es bueno mencionar que las bacterias también aportarían una importante contribución a entender los procesos de diferenciación; un claro ejemplo es el proceso de esporulación donde la bacteria Bacillus subtilis ha sido el modelo vedette [10-11]. También fue en bacterias infectadas por fagos que se pusieron en evidencia los sistemas de restricción-modificación [12-13] tan importantes en las construcciones in vitro.
Los Fagos en los años 70
En los 70, las bacterias, sus fagos y sus plásmidos, condujeron al advenimiento de la Ingeniería Genética (y la Biotecnología). Gracias a los sistemas de recombinación in vitro el grupo de Paul Berg obtuvo los primeros recombinantes inter-reinos utilizando recombinantes entre genes de virus y de bacterias introducidos en cultivos de células (eucariotas) [14]. Esta nueva orientación no fue sin grandes discusiones en el mundo científico lo que en esencia condujo a despertar la responsabilidad de los investigadores por los alcances de sus experimentos y a promover el mejoramiento y control de las condiciones de uso de la tecnología recombinante como surgió de las Reuniones de discusión de Asilomar, 1972 y 1975 [15]. También se promovió la organización de “Comités Consultivos de Ética” donde se convocan no solo a científicos sino también a varios participes políticos y religiosos para opinar y/o decidir sobre el bien-fundado y/o peligrosidad de los experimentos, antes de su realización. Estas posturas y discusiones siguen actualmente a nivel internacional; ejemplo de ellos son el uso de terapias génicas y de organismos genéticamente modificados (OGM) y sus controles.
Los fagos en la actualidad
En los últimos años, los fagos han encontrado su resurrección, ya sea como material de estudio, uso en ciencia básica o por sus posibles aplicaciones.
La alta especificidad de huésped ha permitido su uso en la tipificación de especies; recientemente ha sido posible desarrollar ingeniosas herramientas de diagnóstico [16]
Algunos fagos, como el fago Qbeta con solo 3 genes y un genoma de RNA, son un ejemplo en la utilización de ingeniosas estrategias y economía de medios para su reproducción.
Otros utilizan el sistema SOS del huésped no solo para su escisión como profago, sino también para su reproducción [17]
En fagos también se pusieron en evidencia mecanismos de transposición; un ejemplo de ello es el Fago Mu, capaz de replicar y mutagenizar utilizando la transposición durante su ciclo lítico [18].
La capacidad de multiplicación de los fagos, cientos de veces mayor a la de su hospedador, el uso que hacen de las maquinarias de mutagénesis presentes en ellos y generalmente aumentada por la inducción de la respuesta SOS, la capacidad de superar e incluso apropiarse del sistema de vigilancia que la bacteria utiliza para el reconocimiento y eliminación de secuencias extrañas (CRISPcas), les permite producir una panoplia de fagos adaptables a cualquier cambio del huésped y los convierte en un modelo interesante para estudiar evolución, también en tiempos de laboratorio [19-20-21 ]
Algunos fagos, sobreviven semi-silenciosamente en su huésped (como profagos), pero conllevan en su genoma la información para expresar toxinas y ser los responsables de la patogenicidad de la bacteria portadora (toxinas shigella, cólera, difteria, botulismo) [22 ]. Sin embargo recientemente se empieza a valorar el uso de fagos como alternativa a los antibióticos (fagoterapia), una aplicación que Felix d´Herelle ya había considerado cuando los descubrió y les dio el nombre de bacteriófagos (comedor de bacterias). Esa observación lo condujo a utilizar los lisados de fagos para combatir procesos infecciosos, pero solo fue aceptado y desarrollado en algunos Institutos de la ex URSS [23-24]. En los últimos 10 años, se ha hecho evidente y masificado el interés por su posible potencial terapéutico. Frente a estas dos situaciones: fagos responsables de patogenicidad y fagos destructores de bacterias, uno se puede plantear: ¿Fagos amigos o enemigos, cuándo y para quién? La situación es suficientemente importante como para ser evaluada y analizada en cada situación
¿Cuáles fueron los Principales experimentos y publicaciones que condujeron al nacimiento de la biología molecular?
Sobre la naturaleza del material genético:
-
Mutantes defectivas en la síntesis de vitaminas de la levadura Neurospora transmiten su característica a su descendencia lo que condujo a Beadle, G.W & Tatum en 1941 [25] a formular la hipótesis conocida como: “Un gen, una enzima”
-
El análisis estadístico y de variancia de mutantes de E. coli resistentes al fago virulento T2, permitió a Luria SE & M. Delbrück en 1943 [26] establecer que “Las mutaciones ocurren al azar y espontáneamente” *
-
Los experimentos de Avery OY, MacLeod CM & McCarty en 1944 mostraon el rol esencial del DNA [27]: el DNA aislado de bacterias patógenas (Pneumococcus pneumoniae) trasmiten la patogenicidad a bacterias mutantes no patógenas,
-
El DNA únicamente, sin la intervención de proteínas, es responsable de la transmisión de los caracteres hereditarios. Los experimentos fueron realizados con el fago Lambda y su huésped (E. coli) por Herschey & Chase en 1952. [ 28] *
Estructura de proteínas y del DNA
-
La escuela de los Bragg en Inglaterra con la puesta a punto de la metodología de Rayos X para analizar material biológico, fue muy importante en la determinación de las estructuras de proteínas y luego de ácidos nucleicos [29 ]. Esos estudios permitieron proponer la estructura en alfa-hélice de la hemoglobina por el grupo de Linus Pauling [30] y de la mioglobina por el de Kendrew [31]. A su vez varios equipos emprendieron los análisis de DNAs.
-
Por un lado los análisis químicos realizados por Chargaff, Magasanik, Visher, Gree, Doniger y Elson en 1950 pusieron en evidencia las reglas de apareamiento de bases del DNA de distintos orígenes: ∑ bases púricas (A+T) = ∑ bases pirimídicas (G+C) [32]. Paralelamente, Jim Watson y Francis Crick en Cambridge University, Rosalind Franklin y Maurice Wilkins en el King’s College of London, emprendieron los estudios por difracción de RayosX de DNA de diferente origen. Pero fueron las imágenes obtenidas por R. Franklin[33] que aportaron la prueba más importante para la propuesta de la doble hélice del DNA por el equipo Watson-Crick en 1953 [34]. Sin embargo, R. Franklin no tuvo el reconocimiento merecido por sus colegas; años después numerosos fueron los testimonios tanto en libros como en película destacando su rol.


Figura 4: Rosalind Franklin y la famosa foto 51 obtenida por Difracción de Rayos X del DNA que sirvió a Watson y Crick para proponer el modelo.
Replicación del DNA
-
Demostración del mecanismo de replicación semi-conservativo del DNA realizado con el fago lambda por Meselson M y Stahl FW en 1958 [ 36]*
Recombinación
-
Caracterización de eventos de recombinación (entre fagos) por Hershey AD & M. Chase en 1951[37]* En 1952-53 se pusieron en evidencia sistemas de restricción-modificación importantes en las interacciones entres fagos y bacterias hospedadoras en base a los resultados de Luria & Human [12 ], y Bertani & Weigle [13 ]*
-
La caracterización de fagos capaces de realizar un ciclo lítico o de mantenerse en su huésped en forma atenuada como profago (fagos temperados) permitió caracterizar los procesos de lisogenia donde Lambda fue el modelo vedette (Jacob, Wollman, Lwoff) en 1953 y 1954 [38, 39].
Identificación de mecanismos de transferencia de material genético en bacterias
-
A su vez, Maurice Wilkins, en el mismo laboratorio, aportó datos complementarios [35] que permitieron concretar el modelo en doble hélice del DNA lo que les valdría el premio Nobel a los tres investigadores, Watson, Crick y Wilkins en 1962.
Replicación del DNA
-
Demostración del mecanismo de replicación semi-conservativo del DNA realizado con el fago lambda por Meselson M y Stahl FW en 1958 [ 36]*
Recombinación
-
Caracterización de eventos de recombinación (entre fagos) por Hershey AD & M. Chase en 1951[37]* En 1952-53 se pusieron en evidencia sistemas de restricción-modificación importantes en las interacciones entres fagos y bacterias hospedadoras en base a los resultados de Luria & Human [12 ], y Bertani & Weigle [13 ]*
-
La caracterización de fagos capaces de realizar un ciclo lítico o de mantenerse en su huésped en forma atenuada como profago (fagos temperados) permitió caracterizar los procesos de lisogenia donde Lambda fue el modelo vedette (Jacob, Wollman, Lwoff) en 1953 y 1954 [38, 39].
Identificación de mecanismos de transferencia de material genético en bacterias
-
La conjugación donde la presencia de un plásmido o episoma (F) en una bacteria le permite transferir su genoma, o parte de él, a bacterias no portadoras del F (F-) permitió a Wollman EL, Jacob F & Hayes W en 1956 [40], introducir el concepto de “sexualidad” en bacterias. Por otro lado, la observación de un proceso de lisis durante la conjugación (inducción cigótica) entre cepas de E. coli portadoras o no del profago lambda y el aislamiento de mutantes del fago capaces de controlar ese proceso, fue uno de los ejemplos detonadores de la necesidad de idear controles génicos.
-
La transformación donde el DNA y un estado particular de competencia de la bacteria receptora permite su transferencia: Hotckiss RD. 1951 [42]
-
La transduction donde la bacteria utiliza un fago como vehiculo para transferir DNA del huesped a otra bacteria. Morse ,Lederberg EM & Lederberg J. (1956) [ 41] *
Rol del mRNA y elucidación del código genético
-
Volkin E. & Astrachan L: mostraron la existencia de un RNA intermediario entre el DNA y los ribosomas. (1956) [43] *
-
Se mostraron las características del RNA mensajero.-Brenner S, Jacob F. & Meselson M. (1961) [ 44]
-
Se identificaron los genes responsables de la síntesis de ribosomas:-Yanofsky SA & Spiegelman S. (1962) [45 ] *
-
Se resolvió el código genético y se confirmó la universalidad del mismo gracias a los trabajos de JH Matthaei, OW Jones, RG. Martin, MW. Nirenberg. 1962 [46] Severo Ochoa. 1964. [47 ] y Khorana HG, Büchi H, Ghosh H, Gupta N, Jacob TM, Kössel H, Morgan R, Narang SA, Ohtsuka E, Wells RD. 1966. [48]
-
Marshall W. Nirenberg, J. Heinrich Matthaei. 1961. [49]
-
Tsugita, H. Fraenkel-Conrat, M. W. Nirenberg, J. H. Matthaei. 1962. [50] *
-
Mostraron el rol RNA mensajero (mRNA) como intermediario entre el DNA y los ribosomas y se puso en evidencia el rol de los ribosomas y de los distintos tRNA en el proceso de traducción
Organización genética y procesos regulatorios
-
Se caracterizó la unidad genética mínima de expresión: el cistrón. Un cistrón codifica para una cadena polipeptídica. Un gen (función biológica) puede estar compuesto de varios cistrones. Para ello, se utilizaron mutantes de rango de huésped (rII) del fago T4 que podían desarrollar o no en 2 cepas: E.coli K12 y/o E. coli B (Benzer S, 1955) [51] ) de acuerdo a la composición de cistrones rII y del huésped. *
-
Se propuso el primer sistema de regulación a nivel transcripcional: El operón. Los experimentos de enzimología y mapeo genético realizados en E. coli de diferentes mutantes responsables de la utilización de la lactosa y la obtención de diploides parciales para los genes lac (F´Lac) permitieron postular el primer modelo de regulación a nivel transcripcional: teoría del operón (Jacob, Perrin, Sanchez, Monod 1959; Jacob & Monod 1961) [52-53 ] aplicables a la regulación de los ciclo lítico/ lisogénico del fago λ lambda
-
También es importante mencionar las observaciones y estudios genéticos sobre variabilidad en maíz que condujeron a proponer mecanismos regulatorios de expresión alternativa y movilidad genética (luego transposones) por Barbara McClintock en 1953 [54]. Estos resultados no fueron interpretados en su real dimensión, hasta después de analizar las posibles implicancias de la teoría del operón [55].
* Trabajos en los cuales el sujeto de investigación eran bacteriófagos.
Todos estos trabajos realizados en un periodo de 25 años, la inspiración de sus ejecutores y las intensas colaboraciones que surgieron entre ellos, esencialmente después de la IIda Guerra mundial, conformaron la piedra fundacional para el advenimiento de la biología molecular
Agradecimientos
Quiero agradecer la disponibilidad de fotografías que me han sido brindadas por Emilio Segrè Visual Archives, Cold Spring Harbor laboratory Archives, la familia Delbrück y la “Abbaye de Royaumont"
Agradezco a Sandra Ruzal por sus aportes y apoyo en la realización de este escrito
La autora es investigadora principal de CONICET.
Referencias:
1. D´Herelle F (1917) Sur un microbe invisible antagoniste des bacilles dysentériques Comptes Rendus Académie Sciences Paris 165:373-375
2. Duckworth DH (1976) Who Discovered Bacteriophage?" Bacteriological Review 40: 793-802.
3. Cairns J, Stent GS , Watson JM (2007) Phages and the Origin of Molecular Biology The Centennial Edition Cold Spring Harbor laboratory Press
4. Lederberg EM (1951) Lysogenicity en E. coli K12 Genetics 36 : 560
5. Sanchez de Rivas C. 1968 “Etude de l'effet glucose sur l'opéron lactose d' Escherichia coli K12- Thèse de 3 cycle en Biochimie Université de Paris VI (Noviembre 1968)”.
6. Sanchez de Rivas C, Méndez BS (1976). Catabolite translational effects on the lac messenger RNA of Escherichia coli K12 Molecular and General Geneticsn 18;148:99-104.
7. Beljanski M (1972) Synthèse in vitro de l´ADN sur une matrice d´ARN para une transcriptase d´Escherichia coli Comptes Rendus Académie Sciences. Paris D: 274:2801-4.
8. Temin HM (1972) The RNA tumor viruses-background and foreground Proceeding of the National Academy of Sciences of the United States of America: 69: 1016-20
9. Forterre P , Prangishvili D ( 2009) The origin of viruses Research in Microbiology 160:466-72
10. Stragier P, Losick R (1996) Molecular genetics of sporulation in Bacillus subtilis Annual Review of Genetics 30:297-41.
11. Piggot PJ,Hilbert DW( 2004) Sporulation of Bacillus subtilis Current Opinion in Microbiology 7:579-86.
12. Luria SE, Human ML (1952) A non hereditary, host-induced variation of bacterial viruses Journal of Bacteriology 64:557-69.
13. Bertani G, Weigle J (1953)Host controlled variation in bacterial viruses Journal of Bacteriology 65:113-21
14. Jackson DA, Symons RH , Berg P (1972) Biochemical method for inserting new genetic information into DNA of Simian Virus 40: circular SV40 DNA molecules containing lambda phage genes and the galactose operon of Escherichia coli Proceedings of the National Academy of Sciences of the United States of America 69(10): 2904-9
15. Berg P (2008). Asilomar 1975: DNA modification secured Opinion Nature
16. Piuri M, Jacobs WR Jr , Hatfull GF (2009) Fluoromycobacteriophages for rapid, specific, and sensitive antibiotic susceptibility testing of Mycobacterium tuberculosis PLoS One 4(3):e4870
17. Rubinstein CP, Guerchicoff A , Sanchez-Rivas C (1998). Normal induction of the SOS response in Bacillus subtilis is prevented by the mutant repressor from phage phi105cts23 FEMS Microbiology Letters 167:315-20
18. Toussaint A, Gama MJ, Laachouch J, Maenhaut-Michel G , Mhammedi-Alaoui A (1994) Regulation of bacteriophage Mu transposition Genetica: 93:27-39
19. Forterre P (2006)The origin of viruses and their possible roles in major evolutionary transitions Virus Research 117:5-16.
20. Samson JE, Magadan AH, Moineau S (2015) The CRISPR-Cas Immune System and Genetic Transfers: Reaching an Equilibrium Microbiology Spectrum. F;3(1):PLAS-0034-2014.
21. Samson JE, Magadán AH, Sabri M , Moineau S (2013) Revenge of the phages: defeating bacterial defences Nature Review on Microbiology 11:675-87
22. Tinsley CR, Bille E, Xavier, Nassif X (2006) Bacteriophages and pathogenicity: more than just providing a toxin? Microbes and Infection 8:1365-1371
23. Sulakvelidze A, Alavidze Z, Morris JG Jr (2001) Bacteriophage Therapy Antimicrobial agents and chemotherapy 45: 649–659
24. Chan BK, Abedon ST , Loc-Carrillo C (2013). Phage cocktails and the future of phage therapy Future Microbiology 8:769-83.
25. Beadle GW, Tatum EL (1941). Genetic Control of Biochemical Reactions in Neurospora Proceedings of the National Academy of Sciences of the United States of America 27 : 499–506
26. Luria SE & M. Delbrück (1943). Mutations of bacteria from virus sensitivity to virus resistance Genetics 23 : 491-511
27. Avery OY, MacLeod CM, McCartyM (1944) Studies on the chemical nature of the substance inducing transformation of peumococcal types. Induction of transformation by deoxyribonucleic acid fraction isolated from Pneumococcus Type III Journal of Experimental Medicine 79: 137-158
28. HerscheyA Chase M (1952) Independent functions of viral protein and nucleic acid in growth of bacteriophage Journal of General Physiology 36: 39-56
29. Bragg WL, Kendrew JC, Perutz MF (1950) Polypeptide chain configurations in crystalline proteins Proceeding of the Royal Society of London B Biological Sciences: A 203 (1074): 321.
30. Pauling L, Corey RB, Branson HR (1951) The Structure of Proteins: Two Hydrogen-Bonded Helical Configurations of the Polypeptide Chain Proceedings of the National Academy of Sciences of the United States of America 37 205–211.
31. Kendrew JC, Bodo G, Dintzis HM, Parrish RG, Wyckoff H , Phillips DC (1958) A three-dimensional model of the myoglobin molecule obtained by X-ray analysis Nature 181:662-66
32. Chargaff E, Magasanik B, Visher E, Gree C, Doniger R , Elson D (1950) Nucleotide composition of pentose nucleic acids from yeast and mammalian tissues Jurnal of Biological Chemistry 186:51-67.
33. Watson JD & Crick FHC. 1953. The structure of DNA Cold Spring Harbor Symposia on Quantitative Biology Vol XVIII: 18, 123-131
34. Wilkins MHF, Stokes AR & Wilson HR (1953) Molecular structure of deoxypentose nucleic acids Nature 171: 738-74
35. Franklin R, Gosling RG (1953) Molecular configuratium in sodium thimonucleate Nature 171:740-741
36. Meselson M , Stahl FW (1958). The replication of DNA in Escherichia coli Proceedings of the National Academy of Sciences of the United States of America 44: 671-682
37. Hershey AD , Chase M (1951) Genetic recombination and heterozygosis in bacteriophage Cold Spring Harbor Symposia on Quantitative Biology Vol XVI: 471-450
38. Lwoff A (1953) Lysogeny Bacteriological Reviews 17: 269-337.
39. Jacob F, Wollman E. (1954) Spontaneous induction of the development of bacteriophage in genetic recombination of Escherichia coli K12 Comptes Rendus Académie Sciences,Paris: 239: 317-319
40. Wollman EL, Jacob F, Hayes W (1956) Conjugation and genetic recombination in Escherichia coli K12 Cold Spring Harbor Symposia on Quantitative Biology Volume XXI: 21, 141-162
41. Morse ML, Lederberg EM, Lederberg J (1956) Transduction in Escherichia coli K12 Genetics 41: 142-156
42. Hotckiss RD (1951) Transfer of penicillin resistance in pneumococci by the desoxyribonucleate derived from resistant cultures Cold Spring Harbor Symposia on Quantitative Biology Volume XVI: 16: 457-61
43. Volkin E , Astrachan L (1956) Intracellular distribution of labeled ribonucleic acid after phage infection of Escherchia coli Virology 2 : 433- 437
44. Brenner S, Jacob F, Messelson M (1961) An unstable intermediate carrying information from genes to ribosomes for protein synthesis Nature 190: 576-581
45. Yanofsky SA, Spiegelman S (1962) The identification of the ribosomal RNA cistron by sequence complementarity. II. Saturation and complementarity interaction of the RNA cistron Proceedings of the National Academy of Sciences of the United States of America 48: 1466-1472
46. Matthaei JH, Jones OW, Martin RG ,Nirenberg MW (1962) Characteristics and composition of RNA coding units Proceedings of the National Academy of Sciences of the United States of America 48: 666–677.
47. Ochoa S. 1964. The chemical basis of heredity–the genetic code Bulletin of the New York Academy of Medecine: 40: 387–413.
48. Khorana HG, Büchi H, Ghosh H, Gupta N, Jacob TM, Kössel H, Morgan R, Narang SA, Ohtsuka E Wells RD (1966) Polynucleotide synthesis and the genetic code Cold Spring Harbor Symposia on Quantitative Biology 31:39-49
49. Nirenberg MW, Matthaei JH (1961) The dependence of cell- free protein synthesis in E. coli upon naturally occurring or synthetic polyribonucleotides Proceedings of the National Academy of Sciences of the United States of America 47: 1588–1602.
50. Tsugita A, Fraenkel-Conrat H, Nirenberg MW & Matthaei JH (1962) Demonstration of the messenger role of viral RNA Proceedings of the National Academy of Sciences of the United States of America 48: 846–853.
51. Benzer S (1955). Fine structure of a genetic region in bacteriophage Proceedings of the National Academy of Sciences of the United States of America 41: 344- 354
52. Jacob F, Perrin D, Sanchez C, Monod J (1960) L´opéron: groupe de gènes à expression coordonnée par un opérateur Comptes Rendus Académie Sciences,Paris 250: 1727-1729
53. Jacob F, Monod J (1961) Genetic regulatory mechanisms in the control of protein synthesis Journal of Molecular Biology 3: 318-356
54. McClintock B (1953) Induction of Instability at Selected Loci in Maize Genetics 38: 579–599
55. McClintock B (1961) Some Parallels Between Gene Control Systems in Maize and in Bacteria The American Naturalist 95 : 265–277.
|
Revista QuímicaViva Número 3, año 14, Diciembre 2015 quimicaviva@qb.fcen.uba.ar |